Iklan
Pertanyaan
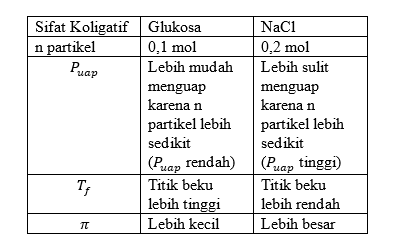
Dua gelas kimia, A dan B diisi dengan air suling sebanyak 100 mL, kemudian ke dalam gelas kimia A dilarutkan 18 gram glukosa, C 6 H 12 O 6 , dan ke dalam gelas B dilarutkan 5,85 gram serbuk garam dapur, NaCl. Untuk kedua larutan yang dihasilkan, perhatikan pernyataan-pernyataan berikut: 1. Pelarut pada gelas A lebih mudah menguap daripada gelas B 2. Jumlah partikel terlarut pada gelas A sama dengan pada gelas B 3. Titik beku larutan pada gelas A lebih tinggi daripada gelas B 4. Tekanan osmotik larutan pada gelas A sama dengan pada gelas B Pernyataan yang benar adalah .... (diketahui Ar H=1, O=16, Na=23, Cl-35,5)
Dua gelas kimia, A dan B diisi dengan air suling sebanyak 100 mL, kemudian ke dalam gelas kimia A dilarutkan 18 gram glukosa, , dan ke dalam gelas B dilarutkan 5,85 gram serbuk garam dapur, NaCl. Untuk kedua larutan yang dihasilkan, perhatikan pernyataan-pernyataan berikut:
1. Pelarut pada gelas A lebih mudah menguap daripada gelas B
2. Jumlah partikel terlarut pada gelas A sama dengan pada gelas B
3. Titik beku larutan pada gelas A lebih tinggi daripada gelas B
4. Tekanan osmotik larutan pada gelas A sama dengan pada gelas B
Pernyataan yang benar adalah .... (diketahui Ar H=1, O=16, Na=23, Cl-35,5)
1 dan 2
1 dan 3
2 dan 3
2 dan 4
3 dan 4
Iklan
S. Lubis
Master Teacher
7
5.0 (5 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia