Iklan
Pertanyaan
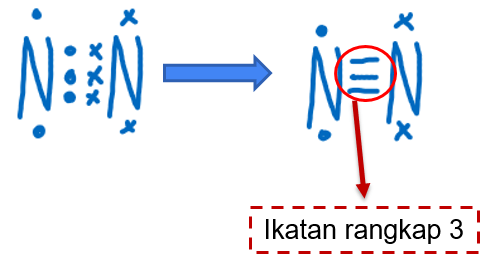
Diketahui nomor atom: 1 H , 7 N , 8 O , 9 F , 17 Cl .Molekul berikut ini yang berikatan kovalen rangkap tiga adalah....
Diketahui nomor atom: . Molekul berikut ini yang berikatan kovalen rangkap tiga adalah....
Iklan
SO
S. Of
Master Teacher
Jawaban terverifikasi
5
5.0 (2 rating)
ND
Niken Dwi Setyaningrum
Bantu banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia