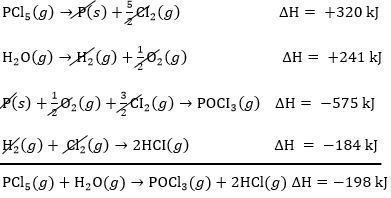Iklan
Pertanyaan
Diketahui: 2 P ( s ) + O 2 ( g ) + 3 CI 2 ( g ) → 2 POCI 3 ( g ) △ H = − 1.150 kJ H 2 ( g ) + Cl 2 ( g ) → 2 HCI ( g ) △ H = − 184 kJ 2 P ( s ) + 5 CI 2 ( g ) → 2 PCl 5 ( g ) △ H = − 640 kJ 2 H 2 ( g ) + O 2 ( g ) → 2 H 2 O ( g ) △ H = − 482 kJ Hitunglah △ H untuk reaksi: PCl 5 ( g ) + H 2 O ( g ) → POCl 3 ( g ) + 2 HCl ( g )
Diketahui:
Hitunglah untuk reaksi:
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
3
4.7 (41 rating)
MA
Muhammad Adzikra Raia
Ini yang aku cari!
0
000000000000000000000000ca6082a54b8b16bda7c007f57853264ee5ee2bd8c86c
Mudah dimengerti
SA
Shafa Ainy Haseena Adaby
Pembahasan lengkap banget Ini yang aku cari! Mudah dimengerti Makasih ❤️ Bantu banget
ls
luciana sitorus
Pembahasan tidak menjawab soal
IR
Inaya Rizka Khairunika
Mudah dimengerti Makasih ❤️ Bantu banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia