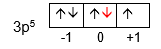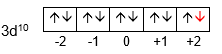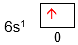Iklan
Iklan
Pertanyaan
Diketahui harga keempat bilangan kuantum elektron terakhir dari unsur A, B, dan C sebagai berikut. a . A : n = 3 , l = 1 , m = 0 , dan s = − 2 1 b . B : n = 3 , l = 2 , m = + 2 , dan s = − 2 1 c . C : n = 6 , l = 0 , m = 0 , dan s = + 2 1 Tentukan golongan dan periode unsur-unsur tersebut! Unsur manakah yang mempunyai keelektronegatifan paling besar?
Diketahui harga keempat bilangan kuantum elektron terakhir dari unsur A, B, dan C sebagai berikut.
Tentukan golongan dan periode unsur-unsur tersebut! Unsur manakah yang mempunyai keelektronegatifan paling besar?
Iklan
SO
S. Oktasari
Master Teacher
Mahasiswa/Alumni Universitas Padjadjaran
Jawaban terverifikasi
11
2.0 (1 rating)
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia