Iklan
Pertanyaan
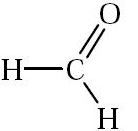
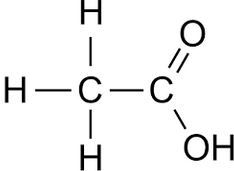
Diketahui dua senyawa yang berbeda A dan B. Analisis unsur menunjukkan kedua senyawa mengandung 40% karbon, 6,7% hidrogen, dan 53,3% oksigen (% massa).Analisis selanjutnya menunjukkan bahwa massa molar senyawa A = 30 , 0 g mol − 1 , sedangkan senyawa B = 60 , 0 g mol − 1 ; Senyawa A dapat dioksidasi oleh kalium permanganat dalam·suasana asam menghasilkan suatu asam, sedangkan senyawa B bereaksi dengan propanol dalam suasana asam sulfat menghasilkan suatu ester. Tentukan struktur serta nama senyawa A dan B.
Diketahui dua senyawa yang berbeda A dan B. Analisis unsur menunjukkan kedua senyawa mengandung 40% karbon, 6,7% hidrogen, dan 53,3% oksigen (% massa). Analisis selanjutnya menunjukkan bahwa massa molar senyawa , sedangkan senyawa ; Senyawa A dapat dioksidasi oleh kalium permanganat dalam·suasana asam menghasilkan suatu asam, sedangkan senyawa B bereaksi dengan propanol dalam suasana asam sulfat menghasilkan suatu ester. Tentukan struktur serta nama senyawa A dan B.
Iklan
Q. 'Ainillana
Master Teacher
Mahasiswa/Alumni Universitas Negeri Yogyakarta
2
4.8 (8 rating)
Brilian Nugraha Siwi
Bantu banget Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia