Iklan
Pertanyaan
Di bawah ini adalah kurva PV/RT terhadap P, untuk gas ideal dan gas non-ideal. P adalah tekanan gas, V adalah volume gas, R adalah tetapan gas ideal dan T adalah temperatur. Dari gas-gas berikut ini yang akan memberikan deviasi (penyimpangan) paling besar dari sifat gas ideal adalah ….
Di bawah ini adalah kurva PV/RT terhadap P, untuk gas ideal dan gas non-ideal.
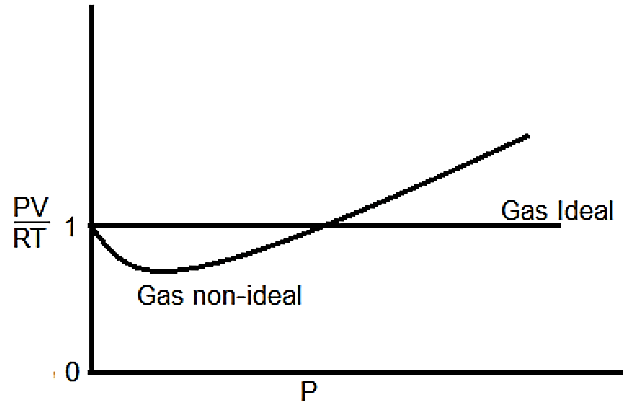
P adalah tekanan gas, V adalah volume gas, R adalah tetapan gas ideal dan T adalah temperatur. Dari gas-gas berikut ini yang akan memberikan deviasi (penyimpangan) paling besar dari sifat gas ideal adalah ….
metana (
)
etana (
)
helium (He)
belerang dioksida (
)
etena (
)
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
2
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















