Gaya dispersi atau gaya london adalah gaya tarik menarik antara dipol sementara. Dipol sementara terbentuk karena molekul yang tidak memiliki dipol terinduksi sehingga menyebabkan munculnya dipol positif dan negatif yang sifatnya sementara. Suatu molekul disebut tidak memiliki dipol, jika pada molekul tidak terjadi pergeseran kerapatan elektron. Hal tersebut terjadi pada molekul yang tidak memiliki perbedaan keelektronegatifan dan mungkin juga terjadi pada molekul yang bentuknya simetris.
Molekul yang tidak memiliki perbedaan keelektronegatifan contohnya molekul diatomik dengan atom yang sama. Pada opsi, molekul tersebut adalah O2.
Pada molekul dengan bentuk simetris, untuk mengetahui apakah molekul tersebut tidak memiliki dipol, kita harus melihat pergeseran kerapatan elektronnya. Contoh molekul yang bentuknya simetris adalah CH4. Berikut penggambaran pergeseran kerapatan elektron pada CH4, pergeseran kerapatan elektron ditunjukkan oleh tanda panah.
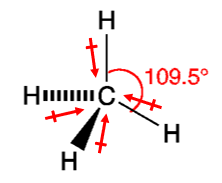
Pergeseran elektron terjadi dari H ke C karena C lebih elektronegatif. Pergeseran kerapatan elektron dari 4 atom H ke atom C akan saling menghilangkan, karena C mengikat 4 atom yang sama dan bentuk molekulnya simetris. Jadi hasilnya pada CH4 tidak terjadi pergeseran kerapatan elektron.
Jadi, molekul yang hanya memiliki gaya london adalah  dan
dan  .
.
Oleh karena itu, jawaban yang benar adalah B.
dan HCl
dan
dan
dan
dan


















