Iklan
Pertanyaan
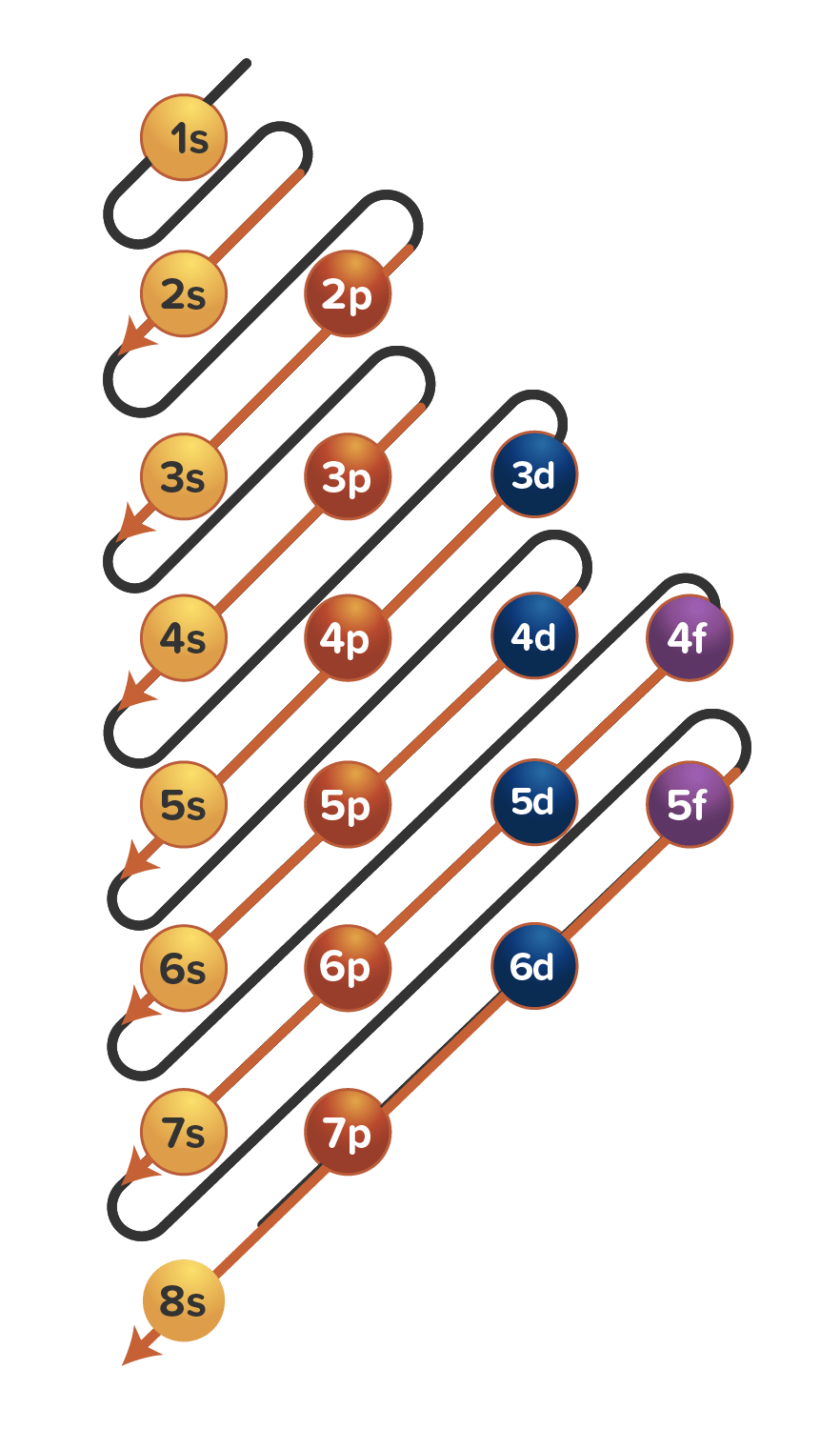
Dengan memperhatikan kestabilan konfigurasi penuh dan setengah penuh, tuliskan konfigurasi elektron dari unsur Mo (Z = 42) dan Ag (Z = 47).
Dengan memperhatikan kestabilan konfigurasi penuh dan setengah penuh, tuliskan konfigurasi elektron dari unsur Mo (Z = 42) dan Ag (Z = 47).
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
5
5.0 (6 rating)
H
Hana
Berkat bantuan kakak, saya bisa mengerti soal ini. Terimakasih kak
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia