Iklan
Pertanyaan
Dengan hanya menggunakan data unsur-unsur dalam tabel periodik di bawah ini, Diketahui bahwa He, Li, C, Si, dan Cl berturut-turut memiliki nomor atom 2, 3, 6, 14, dan 17. Susunlah konfigurasi elektron He, Li, C, Si, dan Cl. Pada tabel di atas, unsur-unsur apa yang terletak pada golongan yang sama? Pada tabel di atas, unsur-unsur apa yang terletak pada periode yang sama? Dalam periode ketiga, atom unsur apa yang memiliki jari-jari atom yang lebih kecil? Atom apa yang memiliki jumlah elektron terbanyak? Atom apa yang paling stabil? Atom apa yang cenderung melepas elektron? Atom apa yang memiliki keelektronegatifan terbesar? Apa kesimpulan yang Anda peroleh dari pertanyaan ini?
Dengan hanya menggunakan data unsur-unsur dalam tabel periodik di bawah ini,
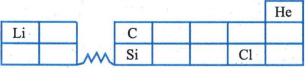
Diketahui bahwa He, Li, C, Si, dan Cl berturut-turut memiliki nomor atom 2, 3, 6, 14, dan 17.
- Susunlah konfigurasi elektron He, Li, C, Si, dan Cl.
- Pada tabel di atas, unsur-unsur apa yang terletak pada golongan yang sama?
- Pada tabel di atas, unsur-unsur apa yang terletak pada periode yang sama?
- Dalam periode ketiga, atom unsur apa yang memiliki jari-jari atom yang lebih kecil?
- Atom apa yang memiliki jumlah elektron terbanyak?
- Atom apa yang paling stabil?
- Atom apa yang cenderung melepas elektron?
- Atom apa yang memiliki keelektronegatifan terbesar?
- Apa kesimpulan yang Anda peroleh dari pertanyaan ini?
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
4
5.0 (2 rating)
SD
Sang Dewi
Bantu banget Makasih ❤️
KS
Khoiria Salsabila
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















