Iklan
Pertanyaan
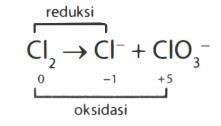
Dalam suasana basa, Cl 2 mengalami reaksi disproporsionasi menghasilkan ion CI − dan ion ClO 3 − . Jumlah mol ion ClO 3 − yang dihasilkan dari 1 mol Cl 2 adalah ...
Dalam suasana basa, mengalami reaksi disproporsionasi menghasilkan ion dan ion . Jumlah mol ion yang dihasilkan dari 1 mol adalah ...
1/5
1/3
1/2
1
2
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
1
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia