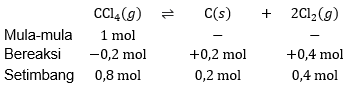Iklan
Pertanyaan
Dalam ruang bervolume 1 L sebanyak 1 mol gas CCl 4 terurai 20% menurut reaksi: CCl 4 ( g ) ⇌ C ( s ) + 2 Cl 2 ( g ) Harga K p reaksi tersebut pada suhu 27 ∘ C sebesar .... ( R = 0 , 082 L atm mol − 1 K − 1 )
Dalam ruang bervolume 1 L sebanyak 1 mol gas terurai 20% menurut reaksi:
Harga reaksi tersebut pada suhu sebesar ....
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
1
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia