Iklan
Iklan
Pertanyaan
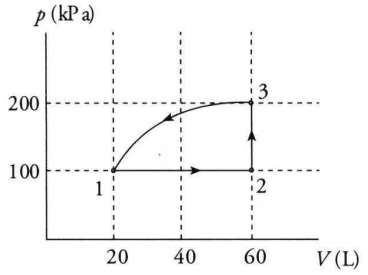
Dalam gambar, suatu gas ideal semula mengalami proses isobarik dari keadaan 1 ke keadaan 2 dengan menyerap kalor 10 kJ, kemudian mengalami proses isokhorik dari keadaan 2 ke keadaan 3 dengan menyerap kalor sebesar 11 kJ. Jika energi dalam pada keadaan 1 adalah U 1 = 5 kJ, tentukanlah U 2 !
Dalam gambar, suatu gas ideal semula mengalami proses isobarik dari keadaan 1 ke keadaan 2 dengan menyerap kalor 10 kJ, kemudian mengalami proses isokhorik dari keadaan 2 ke keadaan 3 dengan menyerap kalor sebesar 11 kJ. Jika energi dalam pada keadaan 1 adalah U1 = 5 kJ, tentukanlah U2!
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
1
5.0 (1 rating)
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia
















