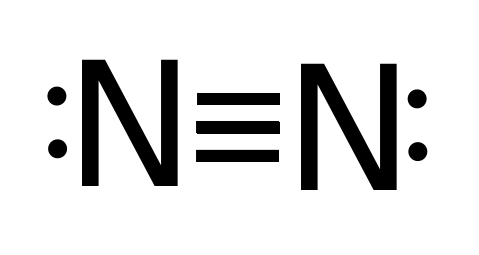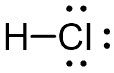Ikatan kovalen terbentuk dari atom nonlogam dan nonlogam. Ikatan kovalen ini terjadi akibat adanya penggunaan elektron bersama. Jika suatu ikatan terbentuk dari adanya serah terima elektron antara logam dan nonlogam, ikatan tersebut disebut sebagai ikatan ionik.
Berikut ini analisis ikatan dari kelima opsi jawaban.
 (Na = logam, Cl = nonlogam)
(Na = logam, Cl = nonlogam)  ikatan ionik
ikatan ionik (2 atom N = nonlogam)
(2 atom N = nonlogam)  ikatan kovalen
ikatan kovalen (H = nonlogam, Cl = nonlogam)
(H = nonlogam, Cl = nonlogam)  ikatan kovalen
ikatan kovalen (K = logam, Br = nonlogam)
(K = logam, Br = nonlogam)  ikatan ionik
ikatan ionik (Ca = logam, Cl = nonlogam)
(Ca = logam, Cl = nonlogam)  ikatan ionik
ikatan ionik
Dengan demikian, senyawa yang memiliki ikatan kovalen adalah  dan HCl. Untuk mengetahui jenis ikatan kovalennya, perlu digambarkan struktur Lewis dari tiap-tiap senyawa.
dan HCl. Untuk mengetahui jenis ikatan kovalennya, perlu digambarkan struktur Lewis dari tiap-tiap senyawa.
Opsi B. 
Nomor atom N = 17. Konfigurasi elektronnya sebagai berikut.

Atom N memiliki 5 elektron valensi. Untuk mencapai keadaan stabil (oktet), satu atom N memerlukan 3 elektron lagi yang diperoleh dari penggunaan bersama elektron antaratom N. Dengan demikian, senyawa  mempunyai ikatan rangkap tiga dengan struktur Lewisnya sebagai berikut.
mempunyai ikatan rangkap tiga dengan struktur Lewisnya sebagai berikut.
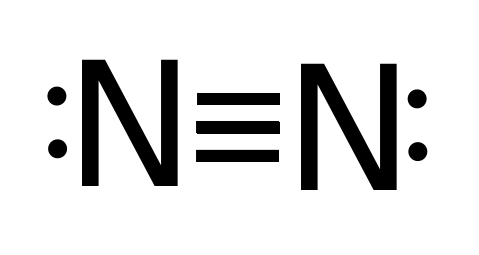
Opsi C. HCl
Senyawa HCl terdiri dari 1 atom H dan 1 atom Cl. Nomor atom H adalah 1 dengan konfigurasi elektron sebagai berikut.

Atom H memiliki 1 elektron valensi. Untuk mencapai keadaan stabil (duplet), atom H memerlukan 1 elektron lagi.
Nomor atom Cl = 17 dengan konfigurasi sebagai berikut.

Atom Cl memiliki 7 elektron valensi. Untuk mencapai keadaan stabil (oktet), atom Cl memerlukan 1 elektron lagi.
Senyawa HCl terbentuk akibat penggunaan bersama 1 elektron dari atom Cl dan 1 elektron dari atom H. Dengan demikian, senyawa HCl yang terbentuk mempunyai ikatan tunggal dan struktur Lewisnya dapat digambarkan sebagai berikut.
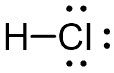
Jadi, jawaban yang tepat adalah C.