Iklan
Pertanyaan
Adit melakukan percobaan di sekolah dengan mereaksikan logam dengan larutan asam. Terdapat dua logam yang akan direaksikan, yaitu logam magnesium (Mg) dan tembaga (Cu) yang akan diuji untuk direaksikan masing-masing dengan larutan H₂SO₄ dan ZnCl₂. Hasil percobaan diperoleh data sebagai berikut: Dari data percobaan dapat disimpulkan, meningkatnya daya oksidasi logam yaitu ....
Adit melakukan percobaan di sekolah dengan mereaksikan logam dengan larutan asam. Terdapat dua logam yang akan direaksikan, yaitu logam magnesium (Mg) dan tembaga (Cu) yang akan diuji untuk direaksikan masing-masing dengan larutan H₂SO₄ dan ZnCl₂. Hasil percobaan diperoleh data sebagai berikut:
Dari data percobaan dapat disimpulkan, meningkatnya daya oksidasi logam yaitu ....
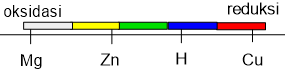
Mg-Zn-H-Cu
H-Cu-Mg-Zn
Mg-Zn-Cu-H
Cu-Mg-Zn-H
Cu-H-Mg-Zn
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
1
5.0 (2 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia