IN
Icha N
16 Mei 2022 15:20
Iklan
IN
Icha N
16 Mei 2022 15:20
Pertanyaan
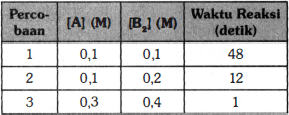
Untuk reaksi yang sesuai dengan persamaan kimia: 2A(g) + B2(g) → C(g) + D(g) diperoleh data percobaan laju reaksi sebagai berikut: Jika dilakukan percobaan dengan [A] = 0,2 M dan [B] = 0,3 M, waktu reaksinya adalah ... (A) 48/18 detik (B) 48/9 detik (C) 8 detik (D) 48 detik (E) 288 detik
2
1
Iklan
SZ
S. Zulaihah
Mahasiswa/Alumni Universitas Negeri Surabaya
17 Mei 2022 00:23
Jawaban terverifikasi
Jawaban yang benar adalah A. 48/18 detik. Laju reaksi merupakan laju perubahan konsentrasi zat-zat komponen reaksi setiap satuan waktu. Dalam laju reaksi, dikenal istilah orde reaksi. Orde reaksi merupakan hubungan antara perubahan konsentrasi dengan perubahan laju reaksi. Pada data percobaan diatas, orde reaksi P dan Q dapat ditentukan dengan cara sebagai berikut. Karena laju reaksi berbanding terbalik terhadap waktu, maka v = 1/t, sehingga v1/v2 = t2/t1 1. Orde reaksi B2 Untuk menentukan orde reaksi B2, maka perlu mencari data konsentrasi A yang sama (tetap), yaitu pada data percobaan 1 dan 2. v1 / v2 = ([B2]1 / [B2]2)^y t2 / t1 = ([B2]1 / [B2]2)^y (12 / 48) = (0,1 / 0,2)^y (1/4) = (1/2)^y (1/2)² = (1/2)^y y = 2 2. Orde reaksi A Untuk menentukan orde reaksi A, maka perlu mencari data konsentrasi B yang sama (tetap). Namun, karena konsentrasi B berbeda semua, maka bisa mengambil data acak dimana konsentrasi A dan B masing-masing berbeda (tidak boleh ada data yang sama) Misal pada data percobaan 1 dan 3. v1 / v3 = ([A]1 / [A]3)^x ([B2]1 / [B2]3)^y t3 / t1 = ([0,1] / [0,3])^x (0,1 / 0,4)² (1/48) = (1/3)^x (1/4)² (1/48) = (1/3)^x (1/16) (1/3) = (1/3)^x x = 1 Persamaan laju reaksinya adalah v = k [A]¹[B2]² v = k [A][B2]² nilai k dapat ditentukan sebagai berikut. ▪︎mengambil salah satu data, misalkan data 1. v = k [A][B2]² 1/t = k (0,1 M)(0,1 M)² 1/48 = k × 0,001 k = 1000/48 Jika dilakukan percobaan dengan [A] = 0,2 M dan [B] = 0,3 M, waktu reaksinya adalah v = k [A][B2]² 1/t = 1000/48 (0,2 M)(0,3 M)² 1/t = (1000/48)(2/10)(9/100) 1/t = 18/48 t = 48/18 detik Jadi, waktu reaksinya adalah 48/18 detik.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



