AM
Andi M
23 Juni 2022 13:05
Iklan
AM
Andi M
23 Juni 2022 13:05
Pertanyaan
untuk mengetahui konsentrasi asam sulfat h2so4 yang belum diketahui seorang mahasiswa melakukan percobaan di laboratorium kimia. percobaan yang dilakukan adalah titrasi asam oleh basa. mahasiswa tersebut mengambil 50ml asam sulfat kemudian diencerkan dengan air sampai volum larutan tepat 100ml. kemudian mengambil 10ml asam sulfat hasil pengenceran dan dititrasi oleh larutan nh4oh 0,1m (kb nh4oh=10−5).percobaan dilakukan sebanyak 5 kali dan terjadi perubahan warna pada volum ratarata larutan nh4oh20ml.jika larutan nh4oh terus diteteskan pada tabung erlenmeyer, ph larutan hasil titrasi pada penambahan 40ml larutan tersebut adalah...
2
1
Iklan
IY
I. Yassa
24 Juni 2022 01:03
Jawaban terverifikasi
Jawaban: 9 Pada titrasi asam basa terdapat larutan titran (larutan yang diketahui konsentrasinya) dan larutan titrat (larutan yang tidak diketahui konsentrasinya). Larutan titrat diletakkan pada labu Erlenmeyer dan diberi indikator untuk mengindikasi titik ekuivalen tercapai dengan perubahan warna. Titik ekuivalen terjadi jika mol asam habis bereaksi dengan mol basa. Menentukan Konsentrasi Asam Sulfat atau H2SO4 Konsentrasi H2SO4 dapat diketahui dari data pada saat terjadi perubahan warna (tercapai titik ekuivalen) dengan menggunakan persamaan: a x Ma x Va = b x Mb x Vb dimana: a adalah valensi asam (jumlah ion H⁺), Ma adalah konsentrasi asam (M), Va adalah volume asam (L atau mL), b adalah valensi basa (jumlah ion OH⁻), Mb adalah konsentrasi basa (M), dan Vb adalah volume basa (L atau mL). Reaksi ionisasi H2SO4 dan NH4OH H2SO4 → 2H⁺ + SO4²⁻ (valensi asam= 2) NH4OH ⇌ NH4⁺ + OH⁻ (valensi basa= 1) a x Ma x Va = b x Mb x Vb 2 x Ma x 10 mL = 1 x 0,1 M x 20 mL 20 mL x Ma = 2 mmol Ma= 0,1 M Menentukan pH untuk Volume NH4OH 40 mL Penentuan pH saat keadaan tersebut dapat dengan menggunakan penyangga basa sebab larutan NH4OH (basa lemah) yang ditambahkan berlebih. Pembahasan tersebut ada pada lampiran.

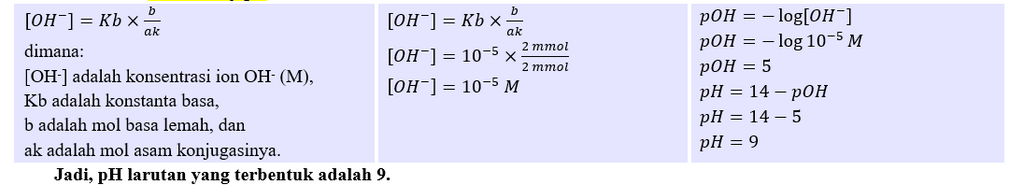
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



