AC
Allisa C
20 Maret 2022 08:14
Iklan
AC
Allisa C
20 Maret 2022 08:14
Pertanyaan
Tuliskan ikatan kovalen antara atom berikut. ₁H dan ₁₆S
2
1
Iklan
DA
D. Aprilia
Mahasiswa/Alumni Universitas Pendidikan Indonesia
21 Maret 2022 08:25
Jawaban terverifikasi
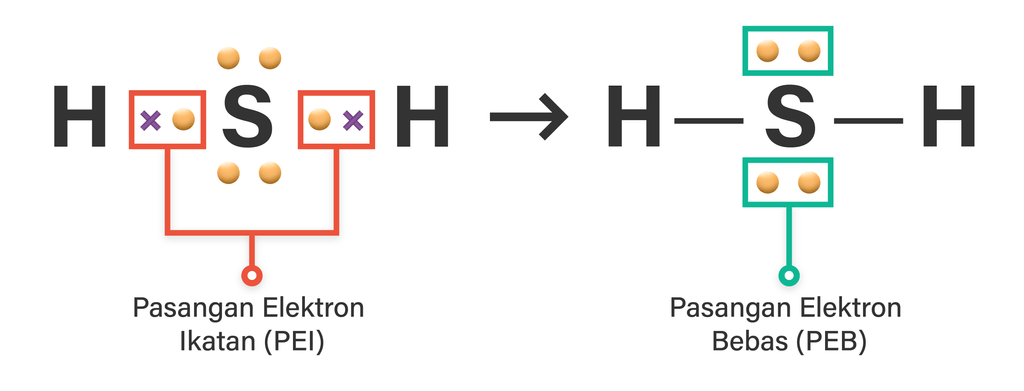
Hai Allisa :) Jadi, ikatan kovalen yang terbentuk antara atom H dengan atom S yaitu kovalen polar dan senyawa yang terbentuk adalah H2S. Agar lebih paham, yuk simak pembahasan berikut ini! Berdasarkan unsur penyusunnya, ikatan kovalen tersusun atas unsur nonlogam dan nonlogam. Ikatan kovalen terbentuk karena adanya pemakaian bersama pasangan elektron. Untuk menentukan ikatan kovalen dari 2 unsur, kita tuliskan dahulu elektron valensinya. Elektron valensi merupakan elektron terluar yang bisa kita ketahui dari nomor atomnya. 1H = 1 (elektron valensi 1, membutuhkan 1 elektron untuk memenuhi kaidah duplet) 16S = 2 8 6 (elektron valensi 6, cenderung menangkap 2 elektron agar memenuhi kaidah oktet) karena atom S membutuhkan 2 elektron lagi, artinya harus terdapat 2 atom H yang mana setiap elektron valensinya akan berikatan dengan elektron valensi dari atom S. Sehingga ikatan kovalen yang terbentuk : H–S–H Untuk lebih jelasnya perhatikan gambar dibawah. Elektron valensi atom H disimbolkan ”x” sedangkan untuk atom S disimbolkan bulatan kuning. Terdapat 2 PEI dan 2 PEB pada atom S sebagai atom pusat. Adanya PEB pada atom pusat menyebabkan senyawa H2S ini termasuk kovalen polar (berikatan kovalen polar).
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



