AC
Annisa C
26 Januari 2022 03:46
Iklan
AC
Annisa C
26 Januari 2022 03:46
Pertanyaan
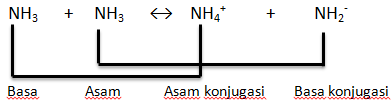
Tuliskan asam-basa konjugat untuk reaksi berikut. NH3 + NH3 ⇌ NH4^+ + NH2^-
9
1
Iklan
LN
L. Ngl
07 Februari 2022 12:10
Jawaban terverifikasi
Hi, Annisa C. Kakak bantu jawab ya. Jawaban yang benar adalah pasangan asam-basa konjugasi yaitu : NH3 dan NH4^+ serta NH3 dan NH2^- Berikut pembahasannya : Asam basa konjugat merupakan teori Asam-Basa Bronsted - Lowry. Asam Bronsted-Lowry adalah zat/spesi yang mendonorkan/memberikan proton (H^+). Suatu asam setelah melepas satu proton (H^+) akan membentuk spesi yang disebut basa konjugat/basa konjugasi. Asam ⇌ Basa konjugasi + H^+ Basa Bronsted-Lowry adalah zat/spesi yang menerima proton (H^+) (akseptor). Suatu basa setelah menerima satu proton (H^+) akan membentuk spesi yang disebut asam konjugat/asam konjugasi. Basa + H^+ ⇌ Asam konjugasi NH3 ⇌ NH2^- + H^+ NH3 berperan sebagai asam karena melepaskan satu proton (H^+) membentuk spesi NH2^- Spesi NH2^- yang terbentuk ini disebut basa konjugasi. NH3 + H^+ ⇌ NH4^+ NH3 berperan sebagai basa karena menyerap satu proton (H^+) membentuk spesi NH4^+ . Spesi NH4^+ yang terbentuk ini disebut asam konjugasi. Dengan demikian pasangan asam-basa konjugasi yaitu : NH3 dan NH4^+ serta NH3 dan NH2^- Berdasarkan persamaan reaksi berikut ini NH3 dapat bersifat sebagai asam (donor proton) dan sebagai basa (akseptor proton). Oleh karena itu NH3 bersifat amfiprotik.
· 5.0 (2)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



