YY
Yolamnda Y
06 Juni 2022 01:41
Iklan
YY
Yolamnda Y
06 Juni 2022 01:41
Pertanyaan
Terdapat senyawa-senyawa berikut: (1 ) NH3 (2) BF3 (3) PCI3 (4) SF4 Diketahui nomor atom: H = 1 ; B = 5 ; N = 7; F = 9; P = 15 ; S = 16 ; Cl = 17 Senyawa yang struktur elektronnya (struktur Lewis) tidak memenuhi kaidah oktet atau duplet adalah (A) 1,2 (B) 1,3 (C) 1,4 (D) 2,3 (E) 2,4
9
1
Iklan
YL
Y. Lutvira
06 Juni 2022 09:07
Jawaban terverifikasi
Jawaban yang benar yang tidak memenuhi kaidah oktet/duplet adalah BF3 dan SF4 (E) Pembahasan Aturan / kaidah oktet menyatakan bahwa suatu unsur dikatakan stabil saat elektron valensinya 8 seperti golongan gas mulia (VIIIA). Setiap unsur selain golongan gas mulia memiliki kecenderungan untuk mencapai kestabilan dengan cara melepas, menangkap, atau memasangkan elektron secara bersama-sama melalui ikatan kimia. Di alam terdapat senyawa-senyawa yang menyimpang dari kaidah oktet. Penyimpangan ini terjadi dikarenakan 3 hal yaitu: 1. Senyawa yang tidak mencapai kaidah oktet, biasanya dimiliki oleh senyawa-senyawa dengan atom pusat yang elektron valensinya kurang dari 4. Misalnya BCl3 2. Senyawa dengan jumlah elektron valensi ganjil, misal N02 3. Senyawa dengan oktet berkembang, yaitu senyawa yang atom pusatnya mempunyai elektron lebih dari 8. Senyawa ini umumnya berasal dari unsur-unsur periode 3, misal : PCl5, SF6. Untuk mengecek suatu senyawa mengikuti aturan oktet atau tidak dapat dilakukan dengan cara sebagai berikut. * Menuliskan konfigurasi elektron BF3 5B = 2 3 9F = 2 7 Berdasarkan konfigurasi elektron di atas, diketahui bahwa elektron valensi atom B adalah 3 dan elektron valensi atom F adalah 7. * Menuliskan struktur lewis BF3 Struktur terlampir Jika diamati, atom F dalam senyawa telah mencapai kaidah oktet (8 elektron), sedangkan atom B hanya terdiri dari 6 elektron. Hal ini termasuk dalam penyimpangan kaidah oktet, dimana atom pusat senyawa tidak mencapai kondisi 8 elektron, tetapi senyawa yang terbentuk stabil. * Menuliskan konfigurasi elektron SF4 16S = 2 8 6 9F = 2 7 Berdasarkan konfigurasi elektron di atas, diketahui bahwa elektron valensi atom S adalah 6 dan elektron valensi atom F adalah 7. * Menuliskan struktur lewis SF4 Struktur terlampir S yang merupakan atom pusat dikelilingi oleh 8 elektron, 6 elektron pada 3 PEI dan 2 elektron pada 1 PEB (ditandai dengan dot berwarna merah). Jadi senyawa yang struktur elektronnya (struktur Lewis) tidak memenuhi kaidah oktet atau duplet adalah BF3 (gambar loading)
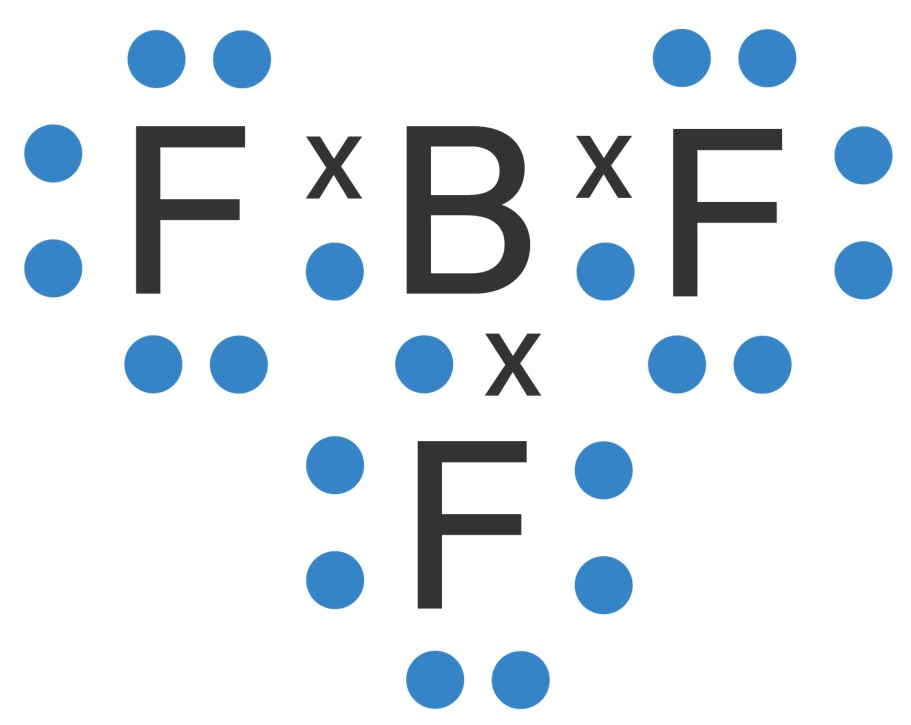
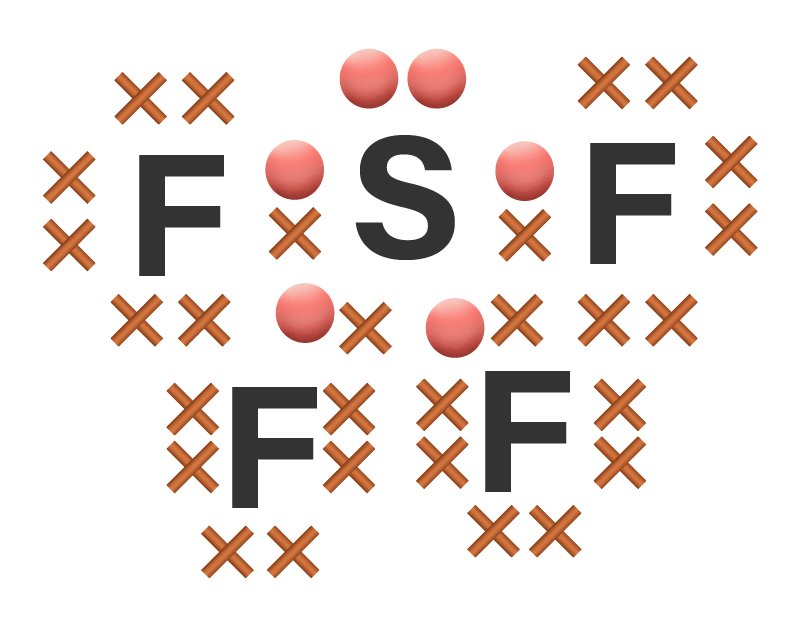
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



