Esra E
01 Februari 2023 10:59
Iklan
Esra E
01 Februari 2023 10:59
Pertanyaan
Tentukan tipe molekul dari SO2
Tentukan tipe molekul dari SO2
6
1
Iklan
J. Siregar
Mahasiswa/Alumni Universitas Negeri Medan
03 Februari 2023 09:37
<p><strong><u>Jawaban yang benar adalah AX</u><sub><u>2</u></sub><u>E (planar bentuk V).</u></strong></p><p> </p><p>Teori domain elektron adalah teori yang menyatakan bahwa pasangan elektron ikatan (PEI) dan pasangan elektron bebas (PEB) saling tolak-menolak. Teori ini dapat digunakan untuk memprediksi bentuk molekul. </p><ul><li>PEI adalah pasangan elektron ikatan yang digunakan untuk berikatan.</li><li>PEB adalah pasangan elektron bebas yang tidak digunakan berikatan. </li></ul><p>Untuk menentukan bentuk molekul menggunakan teori domain elektron, kamu bisa mengacu pada notasi VSEPR AXnEm</p><p>A: atom pusat</p><p>X: pasangan elektron ikatan (PEI)</p><p>n: jumlah PEI dalam molekul</p><p>E: pasangan elektron bebas (PEB)</p><p>m: jumlah PEB dalam molekul</p><p> </p><p>Elektron valensi S dan O dapat diketahui dari konfigurasi elektronnya. </p><p><sub>16</sub>S = 2 8 6 ⇒ elektron valensi = 6</p><p><sub>8</sub>O = 2 6 ⇒ elektron valensi = 6</p><p>Atom S dan O masing-masing memiliki elektron valensi 6. Untuk mencapai kestabilan masing-masing atom S dan O membutuhkan 2 elektron. Atom S mengikat 2 atom O, sehingga salah satu ikatan S dan O adalah ikatan kovalen koordinasi. </p><p>m = ½(elektron valensi - elektron ikatan)</p><p>m = ½(6 - 4) = 1 </p><p>Untuk memperkirakan tipe molekul SO2:</p><ul><li>Atom pusat = S</li><li>Atom terikat = O</li><li>n = 2</li><li>m = 1</li><li>Notasi VSEPR dari SO2 adalah AX<sub>2</sub>E dan geometri molekul planar bentuk V.</li></ul><p> </p><p><strong>Dengan demikian, tipe molekul SO<sub>2</sub> adalah AX<sub>2</sub>E dan geometri molekulnya adalah planar bentuk V.</strong></p>
Jawaban yang benar adalah AX2E (planar bentuk V).
Teori domain elektron adalah teori yang menyatakan bahwa pasangan elektron ikatan (PEI) dan pasangan elektron bebas (PEB) saling tolak-menolak. Teori ini dapat digunakan untuk memprediksi bentuk molekul.
- PEI adalah pasangan elektron ikatan yang digunakan untuk berikatan.
- PEB adalah pasangan elektron bebas yang tidak digunakan berikatan.
Untuk menentukan bentuk molekul menggunakan teori domain elektron, kamu bisa mengacu pada notasi VSEPR AXnEm
A: atom pusat
X: pasangan elektron ikatan (PEI)
n: jumlah PEI dalam molekul
E: pasangan elektron bebas (PEB)
m: jumlah PEB dalam molekul
Elektron valensi S dan O dapat diketahui dari konfigurasi elektronnya.
16S = 2 8 6 ⇒ elektron valensi = 6
8O = 2 6 ⇒ elektron valensi = 6
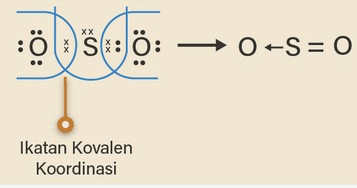
Atom S dan O masing-masing memiliki elektron valensi 6. Untuk mencapai kestabilan masing-masing atom S dan O membutuhkan 2 elektron. Atom S mengikat 2 atom O, sehingga salah satu ikatan S dan O adalah ikatan kovalen koordinasi.
m = ½(elektron valensi - elektron ikatan)
m = ½(6 - 4) = 1
Untuk memperkirakan tipe molekul SO2:
- Atom pusat = S
- Atom terikat = O
- n = 2
- m = 1
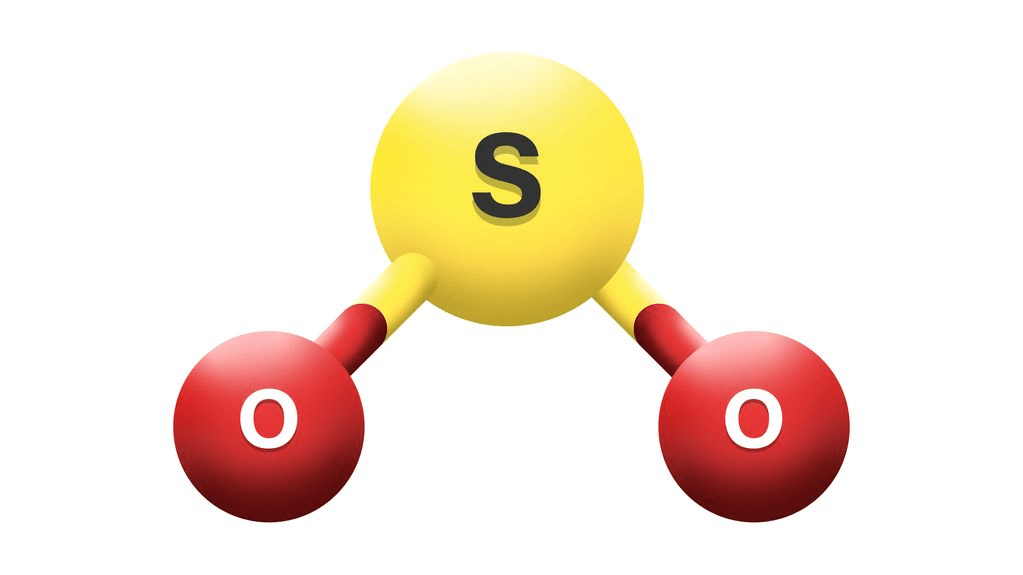
- Notasi VSEPR dari SO2 adalah AX2E dan geometri molekul planar bentuk V.
Dengan demikian, tipe molekul SO2 adalah AX2E dan geometri molekulnya adalah planar bentuk V.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



