Yolamnda Y
15 Januari 2023 05:55
Iklan
Yolamnda Y
15 Januari 2023 05:55
Pertanyaan
Tentukan pH campuran 10 mL NaOH 0,001 M dengan 10 mL CH3COOH 0,001 M (Ka CH3COOH = 1,7 x 10^-5) !
1
1
Iklan
D. Lestari,
Mahasiswa/Alumni Universitas Islam Negeri Maulana Malik Ibrahim Malang
07 Februari 2023 11:05
<p>Jawaban yang benar adalah 7 + log 5,42</p><p> </p><p>Pembahasan</p><p>pH (power Hydrogen) merupakan derajat keasaman. Derajat keasaman ditentukan oleh besarnya konsentrasi ion hidrogen yang ada dalam larutan</p><p>dengan rumus</p><p>pH = -log [H<sup>+</sup>]</p><p>Untuk menentukan pH campuran asam dengan basa, terlebih dahulu membuat reaksi mrs. Sebelumnya tentukan mol masing-masing larutan asam dan basa dengan rumus</p><p>mol = M x V</p><p> </p><p>mol NaOH</p><p>mol = M x V</p><p> = 0,001 M x 10 mL</p><p> = 0,01 mmol</p><p> </p><p>mol CH3COOH</p><p>mol = M x V </p><p> = 0,001 M x 10 mL</p><p> = 0,01 mmol</p><p> </p><p>Reaksi MRS dapat dilihat pada lampiran</p><p> </p><p>Dari persamaan terdapat sisa garam, maka pH ditentukan dengan menggunakan hidolisis</p><p>[CH3COONa] = mol/V</p><p> = 0,01 mmol / 20 mL</p><p> = 0,0005 M</p><p> = 5 x 10^-4 M</p><p>CH3COONa → CH3COO- + Na+</p><p>5 x 10^-4 M 5 x 10^-4 M</p><p> </p><p>[OH-] = √(Kw/Ka) x [anion garam]</p><p> = √(10^-14 / 1,7 x 10^-5) x 5 x 10^-4 M</p><p> = √29,4 x 10^-14</p><p> = 5,42 x 10^-7 M</p><p> </p><p>pOH = - log [OH-]</p><p> = -log 5,42 x 10^-7 M</p><p> = 7 - log 5,42 </p><p> </p><p>pH = 14 - pOH</p><p> = 14 - (7 - log 5,42)</p><p> = 7 + log 5,42</p><p> </p><p>Maka pH campuran larutan tersebut adalah 7 + log 5,42</p>
Jawaban yang benar adalah 7 + log 5,42
Pembahasan
pH (power Hydrogen) merupakan derajat keasaman. Derajat keasaman ditentukan oleh besarnya konsentrasi ion hidrogen yang ada dalam larutan
dengan rumus
pH = -log [H+]
Untuk menentukan pH campuran asam dengan basa, terlebih dahulu membuat reaksi mrs. Sebelumnya tentukan mol masing-masing larutan asam dan basa dengan rumus
mol = M x V
mol NaOH
mol = M x V
= 0,001 M x 10 mL
= 0,01 mmol
mol CH3COOH
mol = M x V
= 0,001 M x 10 mL
= 0,01 mmol
Reaksi MRS dapat dilihat pada lampiran
Dari persamaan terdapat sisa garam, maka pH ditentukan dengan menggunakan hidolisis
[CH3COONa] = mol/V
= 0,01 mmol / 20 mL
= 0,0005 M
= 5 x 10^-4 M
CH3COONa → CH3COO- + Na+
5 x 10^-4 M 5 x 10^-4 M
[OH-] = √(Kw/Ka) x [anion garam]
= √(10^-14 / 1,7 x 10^-5) x 5 x 10^-4 M
= √29,4 x 10^-14
= 5,42 x 10^-7 M
pOH = - log [OH-]
= -log 5,42 x 10^-7 M
= 7 - log 5,42
pH = 14 - pOH
= 14 - (7 - log 5,42)
= 7 + log 5,42
Maka pH campuran larutan tersebut adalah 7 + log 5,42
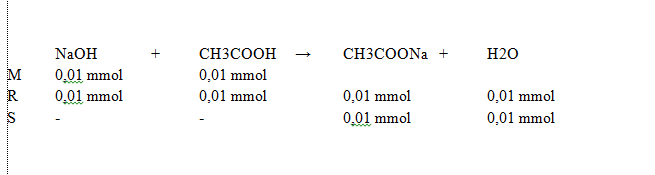
· 5.0 (2)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



