DA
Daniyal A
08 Juni 2021 07:43
Iklan
DA
Daniyal A
08 Juni 2021 07:43
Pertanyaan
Suatu senyawa yang mengandung Ca, N, C, dan S dianalisis secara kuantitatif untuk menentukan rumus molekul senyawa tersebut. Sebanyak 0,250 gram sampel direaksikan dengan Na2CO3 untuk mengubah semua Ca menjadi 0,160 gram kalsium karbonat. Sebanyak 0,115 gram sampel senyawa tersebut direaksikan secara bertahap hingga seluruh S dalam senyawa sampel berubah menjadi 0,344 gram BaSO4. Sedangkan sebanyak 0,712 gram sampel senyawa tersebut diproses sehingga seluruh N lepas menjadi ammonia dan didapatkan massa ammonia yang terbentuk sebanyak 0,155 gram. Setelah dianalisis, senyawa tersebut memiliki massa molekul sebesar 156 gram/mol. Tentukan rumus empiris dan rumus molekul dari senyawa tersebut!
6
1
Iklan
DA
D. Aprilia
Mahasiswa/Alumni Universitas Pendidikan Indonesia
06 Januari 2022 02:53
Jawaban terverifikasi
Halo, Daniyal. Jadi, rumus empiris dan rumus molekul dari senyawa tersebut sama, yaitu Ca(NCS)2. Perhatikan penjelasannya dibawah ini. Penulisan rumus kimia dapat dinyatakan dalam rumus empiris, rumus molekul, dan rumus struktur. Rumus empiris adalah rumus yang menyatakan perbandingan terkecil unsur-unsur yang menyusun suatu-senyawa. Sementara itu, rumus molekul adalah rumus yang menyatakan jumlah unsur-unsur yang menyusun satu molekul senyawa. Rumus molekul merupakan kelipatan dari rumus empiris. Rumus molekul = (Rumus empiris)n Mr Rumus molekul = (Mr Rumus empiris)n, dengan n adalah bilangan bulat Penentuan rumus empiris dan rumus molekul suatu senyawa dapat ditempuh dengan langkah-langkah berikut: a. Mencari massa (persentase) tiap unsur penyusun senyawa. b. Mengubah massa menjadi mol. c. Perbandingan mol paling sederhana dari tiap unsur merupakan rumus empiris. d. Mencari rumus molekul dengan cara berikut: (Mr rumus empiris)n = Mr rumus molekul, n dapat dihitung. e. Mengalikan rumus enipiris dengan n yang diperoleh dari hitungan sehingga diperoleh rumus molekul. Menentukan kadar (%) masing-masing unsur dalam sampel : • Kadar (%) Ca Karena semua Ca dalam sampel diubah menjadi kalsium karbonat CaCO3 sebanyak 0,160 gram dari 0,250 gram sampel, maka massa Ca dalam sampel = massa Ca dalam kalsium karbonat. Perhitungannya sebagai berikut : Diketahui Ar Ca = 40; C = 12; O = 16, maka Mr CaCO3 = 100. 1 atom Ca ≈ 1 molekul CaCO3 1 mol Ca ≈ 1 mol CaCO3 ≈ 100 gram CaCO3 ≈ 40 gram Ca Kadar Ca : (perhatikan gambar ke-1) Kadar (%) S Karena semua S dalam sampel diubah menjadi BasO4 sebanyak 0,344 gram dari 0,115 gram sampel, maka massa S dalam sampel = massa S dalam BaSO4. Dengan perhitungan sebagai berikut : Diketahui Ar Ba = 137; S = 32; O = 16, maka Mr BaSO4 = 233. 1 atom S ≈ 1 molekul BaSO4 1 mol S ≈ 1 mol BaSO4 ≈ 233 gram BaSO4 ≈ 32 gram S Kadar S : (perhatikan gambar ke-2) Kadar (%) N Karena semua N dalam sampel diubah menjadi NH3 sebanyak 0,155 gram dari 0,712 gram sampel, maka massa N dalam sampel = massa N dalam NH3. Dengan perhitungan sebagai berikut : Diketahui Ar N = 14; H = 1, maka Mr NH3 = 17. 1 atom N ≈ 1 molekul NH3 1 mol N ≈ 1 mol NH3 ≈ 17 gram NH3 ≈ 14 gram N Kadar N : (perhatikan gambar ke-3) Kadar (%) C Karena di dalam sampel ada 4 unsur yaitu Ca, N, C dan S, maka yang belum diketahui kadarnya adalah unsur C. sehingga kadar C : Kadar (%) C = 100% - (% Ca + %S + % N) = 100% - (25,6% + 41,08% + 17,93%) = 15,39% Rumus empiris dapat ditentukan dengan menggunakan perbandingan mol unsur-unsurnya: Dengan menganggap massa sampel 100 gram maka : Massa Ca = 25,6 gram; massa N = 17,93 gram; massa C = 15,39 gram dan massa S = 41,08 gram (sesuaikan dengan kadarnya) Maka perbandingan mol Ca, N, C dan S berturut-turut = 25,6/40 ∶ 17,93/14 ∶ 15,39/12 ∶ 41,08/32 = 0,64 ∶ 1,28 ∶ 1,28 ∶ 1,28 Sehingga perbandingan unsur Ca, N, C, dan S adalah 1 : 2 : 2 : 2. Jadi rumus empirisnya adalah CaN2C2S2 atau Ca(NCS)2. Untuk mencari rumus molekul, bisa dengan cara membandingkan Mr RE dengan Mr RM. Dengan menghitung maka Mr RE Ca(NCS)2 = 156. Sedangkan Mr RM atau senyawanya diperoleh dari data soal 156. Karena Mr nya sama maka rumus molekul juga sama yaitu Ca(NCS)2.


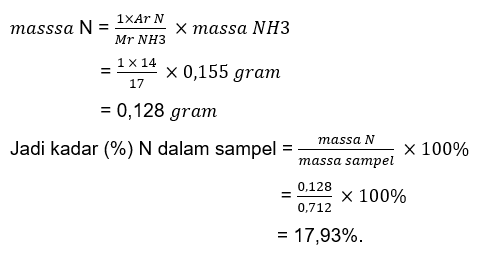
· 5.0 (3)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



