MK
Made K
11 Mei 2022 00:51
Iklan
MK
Made K
11 Mei 2022 00:51
Pertanyaan
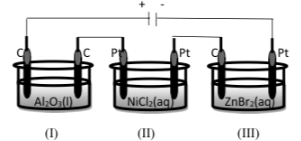
sejumlah arus listrik yang sama besar dialirkan ke dalam rangkaian sel elektrolisis yang disusun seri jika pada sel I dikatode diendapkan 10,8 gram logam aluminium (ar=27), tentukan massa logam yang dihasilkan pada katode di sel III (Ar Ni=58; Zn=65)
2
1
Iklan
SS
S. Susanti
Mahasiswa/Alumni Universitas Jayabaya
11 Mei 2022 21:57
Jawaban terverifikasi
Jawaban yang benar adalah 39 gram seng. Menurut hukum Faraday II, massa zat-zat yang dibebaskan oleh arus listrik yang sama dalam reaksi elektrolisis sama dengan perbandingan massa ekuivalennya. m ≈ ME ME = Ar/biloks Pada gambar di atas dapat diketahui bahwa pada sel I terjadi elektrolisis leburan Al2O3 dan pada sel III merupakan elektrolisis larutan ZnBr2. Langkah pertama yaitu tentukan terlebih dahulu bilangan oksidasi (biloks) dari aluminium (Al) dan seng (Zn) dengan cara membuat reaksi ionisasinya sebagai berikut. Al2O3 --> 2Al3+ + 3O2- ZnBr2 --> Zn2+ + 2Br- Biloks ion monoatom = muatannya, sehingga biloks Al = +3 dan biloks Zn = +2. Langkah selanjutnya, tentukan massa Zn menggunakan persamaan berikut. m Zn / m Al = ME Zn / ME Al m Zn / m Al = (Ar Zn/biloks Zn) / (Ar Al/biloks Al) m Zn / 10,8 g = (65/2) / (27/3) m Zn / 10,8 g = (32,5/9) m Zn = (32,5/9) x 10,8 g m Zn = 39 g Dengan demikian, massa logam yang dihasilkan pada katode di sel III adalah 39 gram seng.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



