CC
Cici C
30 Mei 2022 11:13
Iklan
CC
Cici C
30 Mei 2022 11:13
Pertanyaan
sebanyak 195 gram logam seng / Zn (Ar Zn = 65), yang harus di reaksikan dengan 4 liter larutan asam klorida ( HCl ) 1 M, sesuai reaksi berikut : ...Zn(s) + ....HCl(aq) → ...ZnCl2(aq) + ...H2(g) (reaksi belum setara) Tentukan : a. zat apa yang menjadi pereaksi pembatas (PP)? b. zat apa yang tersisa dan berapa sisanya? c. berapa liter gas hidrogen H2 yang di hasilkan, jika diukur pada suhu 0°C dan tekanan 1 atm?
3
1
Iklan
SZ
S. Zulaihah
Mahasiswa/Alumni Universitas Negeri Surabaya
30 Mei 2022 14:12
Jawaban terverifikasi
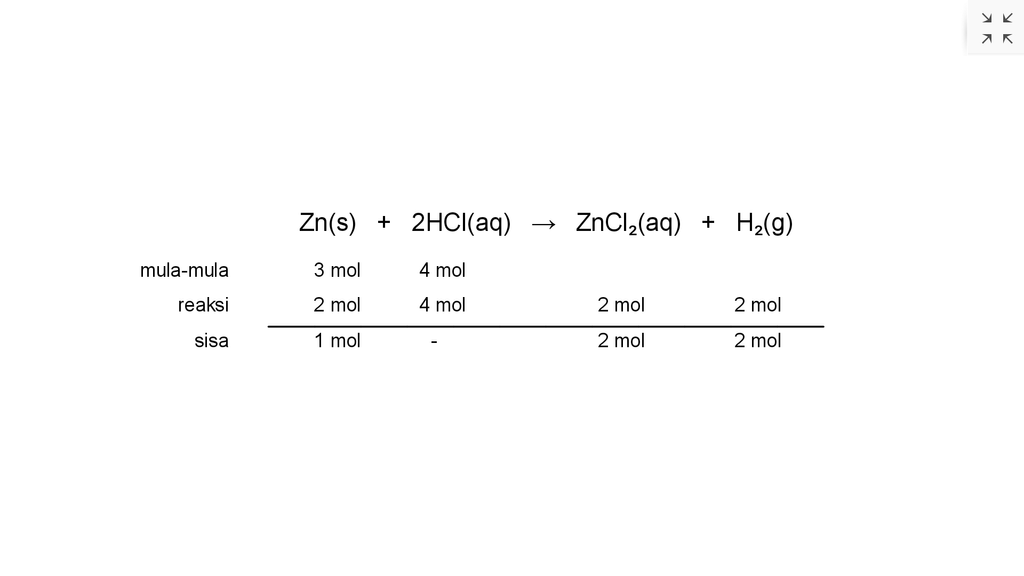
Jawaban yang benar adalah a. HCl b. Zn sebanyak 65 gram c. 44,8 L Di dalam suatu reaksi kimia, perbandingan mol-mol zat pereaksi yang ditambahkan tidak selalu sama dengan perbandingan koefisien reaksinya. Hal ini menyebabkan ada zat pereaksi yang akan habis bereaksi terlebih dahulu. Pereaksi ini disebut pereaksi pembatas. Reaksinya adalah Zn(s) + HCl(aq) → ZnCl₂(aq) + H₂(g) reaksi tersebut belum setara sehingga perlu disetarakan dulu menjadi Zn(s) + 2HCl(aq) → ZnCl₂(aq) + H₂(g) ▪︎menentukan mol masing-masing pereaksi mol Zn = massa / massa molar mol Zn = 195 gram / 65 gram/mol mol Zn = 3 mol mol HCl = M × V mol HCl = 1 M × 4 L mol HCl = 4 mol ▪︎menentukan pereaksi pembatas dengan cara membagi jumlah mol masing-masing pereaksi dengan koesisiennya. a. Zn = mol / koefisien = 3 mol / 1 = 3 b. HCl = mol / koefisien = 4 mol / 2 = 2 Dari perhitungan tersebut, hasil bagi HCl paling kecil sehingga HCl akan habis terlebih dahulu (bertindak sebagai pereaksi pembatas). Reaksi yang terjadi seperti lampiran di bawah ini. Dari reaksi tersebut, zat yang tersisa adalah Zn sebanyak 1 mol. ▪︎menentukan massa Zn yang tersisa mol Zn = massa / massa molar 1 mol = massa / 65 gram/ mol massa = 65 gram ▪︎menentukan volume H₂ pada 0⁰C 1 atm (STP) V H₂ = mol × 22,4 L/mol V H₂ = 2 mol × 22,4 L/mol V H₂ = 44,8 L Jadi, a. Pereaksi pembatasnya adalah HCl. b. Zat yang tersisa adalah Zn yaitu sebanyak 65 gram. c. Volume H₂ pada 0⁰C 1 atm adalah 44,8 L.
· 5.0 (1)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



