VN
Via N
07 Mei 2022 14:36
Iklan
VN
Via N
07 Mei 2022 14:36
Pertanyaan
Sebanyak 100 mL larutan HNO3 0,2 M direaksikan dengan 100 mL KOH 0,1 M. Hitunglah pH campuran.
10
1
Iklan
AA
A. Atikasari
Mahasiswa/Alumni Universitas Negeri Yogyakarta
08 Mei 2022 10:01
Jawaban terverifikasi
Halo Azzahra, kakak bantu jawab pertanyaanmu ya Jawaban: pH = 2 - log 5. Reaksi asam dan basa akan menghasilkan senyawa garam. HNO₃ merupakan asam kuat dan NaOH merupakan basa kuat. Reaksi antara keduanya akan menghasilkan senyawa Garam NaNO₃. Pada soal, reaksi yang terjadi: HNO₃(aq) + NaOH(aq) → NaNO₃(aq) + H₂O(l) ✓ Menentukan mol HNO₃ dan NaOH mol HNO₃ = M x V = 0,2 M x 100 mL = 20 mmol mol NaOH = M x V = 0,1 M x 100 mL = 10 mmol ✓ Reaksi MRS terlampir ✓ Sisa asam = 10 mmol, yang menandakan bahwa larutan bersifat asam. ✓ Menghitung molaritas larutan asam HNO₃ sisa hasil reaksi M HNO₃ = n sisa/V total = 10 mmol/200 mL M HNO₃ = 0,05 M ✓ pH campuran = pH sisa asam Valensi HNO₃ adalah 1, karena hanya melepas 1 ion H+ dalam larutannya, menurut reaksi: HNO₃(aq) --> H+(aq) + NO₃-(aq) [H+] = Ma x a [H+] = 0,05 M x 1 [H+] = 0,05 M = 5 x 10⁻² M pH = - log [H+] pH = - log 5 x 10⁻² pH = 2 - log 5 Jadi, pH campuran yang terbentuk adalah 2 - log 5.
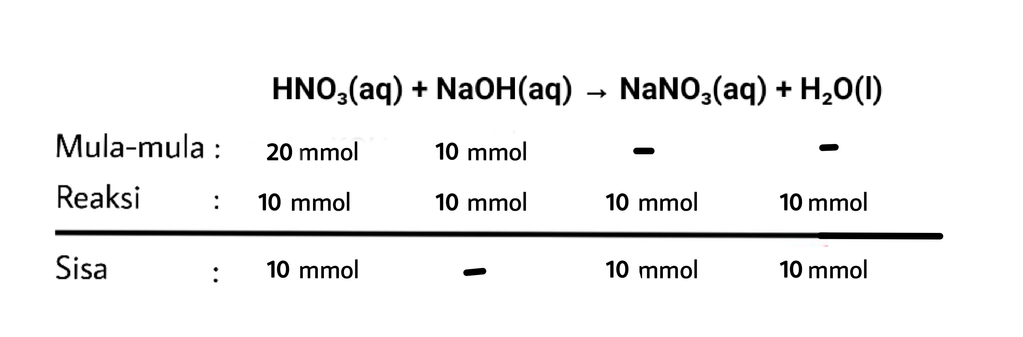
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



