Ana A
13 Agustus 2022 07:32
Iklan
Ana A
13 Agustus 2022 07:32
Pertanyaan
reaksi yang terjadi adalah sebagai berikut: naocl + h2o →hocl +naoh. tentukan zat yang berindak sebagai reduktor dan oksidatornya.
4
1
Iklan
N. Izzatun
Mahasiswa/Alumni Universitas Gadjah Mada
28 September 2022 11:22
<p>Jawabannya : zat yang bertindak sebagai reduktor dan oksidator adalah NaOCl.</p><p> </p><p>Pembahasan :</p><p>Reaksi reduksi adalah reaksi yang ditandai dengan penurunan bilangan oksidasi atom suatu unsur. Sedangkan reaksi oksidasi adalah reaksi yang ditandai dengan kenaikan bilangan oksidasi atom suatu unsur.</p><ul><li>Oksidator = zat yang mengalami reaksi reduksi</li><li>Reduktor = zat yang mengalami reaksi oksidasi</li><li>Hasil reduksi = zat hasil reaksi reduksi</li><li>Hasil oksidasi = zat hasil reaksi oksidasi</li></ul><p> </p><p>Bilangan oksidasi merupakan bilangan yang menandakan jumlah elektron yang dilepas atau diikat oleh atom suatu unsur. Beberapa aturan penentuan bilangan oksidasi (biloks) suatu unsur:</p><ol><li>Jumlah biloks senyawa netral = 0</li><li>Biloks unsur bebas = 0</li><li>Biloks unsur IIA = +2</li><li>Biloks unsur H umumnya = +1, kecuali pada senyawa hidrida = -1</li><li>Biloks unsur O umumnya = -2, kecuali pada senyawa peroksida = -1, superoksida = , OF<sub>2</sub> = +2</li><li>Biloks ion poliatomik = muatan</li></ol><p> </p><p>Pada reaksi NaOCl + H<sub>2</sub>O → HOCl + NaOH, </p><p>Na mengalami penurunan biloks dari dari +3 menjadi +1, artinya mengalami reduksi.</p><p>Cl mengalami kenaikan biloks dari -1 menjadi +1, artinya mengalami oksidasi. </p><p>Sehingga zat NaOCl bertindak sebagai reduktor sekaligus sebagai oksidator.</p><p>→ Perhatikan gambar terlampir.</p><p> </p><p>Jadi, zat yang bertindak sebagai reduktor dan oksidator adalah NaOCl.</p>
Jawabannya : zat yang bertindak sebagai reduktor dan oksidator adalah NaOCl.
Pembahasan :
Reaksi reduksi adalah reaksi yang ditandai dengan penurunan bilangan oksidasi atom suatu unsur. Sedangkan reaksi oksidasi adalah reaksi yang ditandai dengan kenaikan bilangan oksidasi atom suatu unsur.
- Oksidator = zat yang mengalami reaksi reduksi
- Reduktor = zat yang mengalami reaksi oksidasi
- Hasil reduksi = zat hasil reaksi reduksi
- Hasil oksidasi = zat hasil reaksi oksidasi
Bilangan oksidasi merupakan bilangan yang menandakan jumlah elektron yang dilepas atau diikat oleh atom suatu unsur. Beberapa aturan penentuan bilangan oksidasi (biloks) suatu unsur:
- Jumlah biloks senyawa netral = 0
- Biloks unsur bebas = 0
- Biloks unsur IIA = +2
- Biloks unsur H umumnya = +1, kecuali pada senyawa hidrida = -1
- Biloks unsur O umumnya = -2, kecuali pada senyawa peroksida = -1, superoksida = , OF2 = +2
- Biloks ion poliatomik = muatan
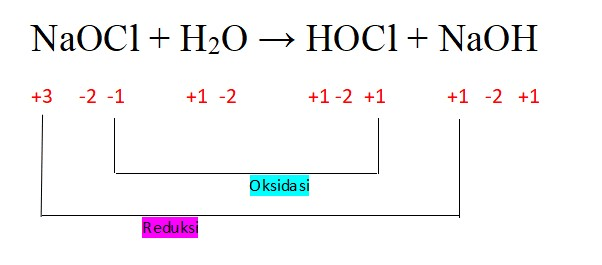
Pada reaksi NaOCl + H2O → HOCl + NaOH,
Na mengalami penurunan biloks dari dari +3 menjadi +1, artinya mengalami reduksi.
Cl mengalami kenaikan biloks dari -1 menjadi +1, artinya mengalami oksidasi.
Sehingga zat NaOCl bertindak sebagai reduktor sekaligus sebagai oksidator.
→ Perhatikan gambar terlampir.
Jadi, zat yang bertindak sebagai reduktor dan oksidator adalah NaOCl.
· 0.0 (0)
Dhyxie D
18 Juli 2023 14:25
Kenapa Na biloksnya +3? Bukankah aturan setiap unsur golongan 1A biloksnya = +1 ? Makasih
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



