NN
Naufan N
29 Juni 2022 09:26
Iklan
NN
Naufan N
29 Juni 2022 09:26
Pertanyaan
pH campuran 100ml larutan NH3 0,2M dengan 100ml larutan HCl 0,1M. kb NH3=10^(−6) adalah ....a 5
4
1
Iklan
YY
Y. Yeni
Mahasiswa/Alumni Universitas Negeri Padang
30 Juni 2022 00:39
Jawaban terverifikasi
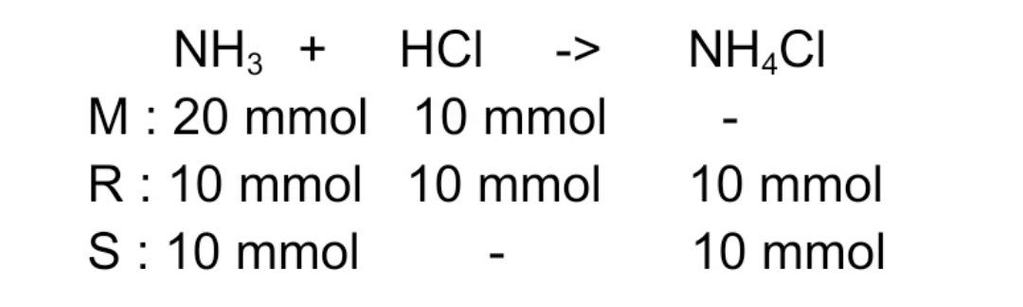
Jawaban : pH larutan = 8 Larutan penyangga merupakan larutan yang dapat mempertahankan pH walau ditambah sedikit asam, basa atau air. Salah satu larutan penyangga yaitu larutan penyangga basa. Menghitung pH larutan penyangga basa yaitu [OH⁻] = Ka x ( mol basa lemah / mol garam) NH₃, basa lemah dan HCl asam kuat bereaksi akan membentuk garam NH₄Cl Mol NH₃ = M x V = 0,2 M x 100 mL = 20 mmol Mol HCl = M x V = 0,1 M x 100 mL = 10 mmol Mol NH₄Cl = mol HCl = 10 mmol [OH⁻] = Kb x ( mol basa lemah / mol garam) = 10⁻⁶ x ( 10 mmol/10 mmol ) = 10⁻⁶ pOH = - log [OH⁻] = - log 10⁻⁶ = 6 pH = 14 - pOH = 14 - 6 = 8 Jadi, pH larutan yang terbentuk adalah 8.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



