Shaquillah H
25 November 2023 17:02
Iklan
Shaquillah H
25 November 2023 17:02
Pertanyaan
Perhatikan reaksi redoks (setara) di bawah ini ! 2KMnO4(aq) + 16HCl(aq) → 2MnCl2(aq) + 5Cl2(g) + 2KCl(aq) + 8H2O(l) Jika reaksi tersebut menghasilkan 5,6 liter gas klorin (STP), maka hitunglah massa kalium permanganat yang digunakan pada reaksi tersebut ! (Mr KMnO4 = 158)

1
1
Iklan
MABAFKUI M
26 November 2023 04:36
<p>hallo izin menjwab yaa cmiiw,🤗</p><p>langkah langkah: </p><p>1. reaksi sudah setara jadi tidak perlu disetarakan</p><p>2. lihat perbandingan koefisien antara senyawa yang diketahui dan senyawa yang ditanyakan di soal</p><p>3. tulis angka perbandingan unsur tersebut untuk menghitung jumlah mol yang bereaksi(sesuai koefisien)</p><p>4. hitung mol dari senyawa yang diketahui volumenya dengan rumus gas STP yaitu V = n x 22,4</p><p>5. setelah ketemu molnya maka bandingkan koefisien senyawa KMnO4 dengan Cl2 yaitu 2:5, berarti mol untuk KMnO4 nya adalah 2/5 dari mol Cl2</p><p>6. langkah terakhir yaitu menghitung massa KMnO4 dengan rumus, massa = mol x Mr </p><p> </p>
hallo izin menjwab yaa cmiiw,🤗
langkah langkah:
1. reaksi sudah setara jadi tidak perlu disetarakan
2. lihat perbandingan koefisien antara senyawa yang diketahui dan senyawa yang ditanyakan di soal
3. tulis angka perbandingan unsur tersebut untuk menghitung jumlah mol yang bereaksi(sesuai koefisien)
4. hitung mol dari senyawa yang diketahui volumenya dengan rumus gas STP yaitu V = n x 22,4
5. setelah ketemu molnya maka bandingkan koefisien senyawa KMnO4 dengan Cl2 yaitu 2:5, berarti mol untuk KMnO4 nya adalah 2/5 dari mol Cl2
6. langkah terakhir yaitu menghitung massa KMnO4 dengan rumus, massa = mol x Mr
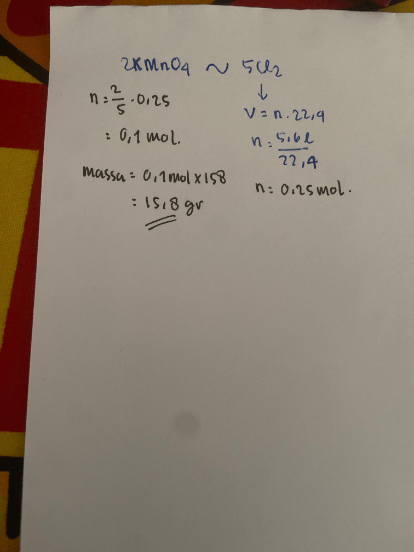
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



