MM
Maria M
11 April 2022 01:44
Iklan
MM
Maria M
11 April 2022 01:44
Pertanyaan
Perhatikan reaksi dalam larutan aqua berikut I⁻(aq) + OCl⁻(aq) → IO⁻(aq) + Cl⁻(aq) Data konsentrasi awal dan laju awal reaksi di atas adalah sebagai berikut : Tentukan hukum laju untuk reaksi tersebut!
5
1
Iklan
AC
A. Chusna
03 Agustus 2022 03:22
Jawaban terverifikasi
Jawaban dari pertanyaan di atas adalah V = k [I⁻][OCl⁻]. Hal pertama yang dilakukan untuk mengetahui hukum laju reaksi adalah menentukan orde reaksi pada reaktan. Orde reaksi dapat ditentukan dengan cara membandingkan laju reaksi hasil percobaan. I⁻(aq) + OCl⁻(aq) → IO⁻(aq) + Cl⁻(aq) Persamaan laju reaksi dari reaksi di atas adalah V = k [I⁻]ⁿ[OCl⁻]ⁱ, dengan n merupakan orde reaksi terhadap I⁻ dan i merupakan orde reaksi terhadap OCl⁻. - Menentukan orde reaksi terhadap I⁻ Orde reaksi terhadap I⁻ (n) dapat ditentukan dengan cara membandingkan laju reaksi pertama dan kedua. Orde reaksi I⁻ adalah 1. ( Hasil perhitungan terlampir dalam gambar) - Menentukan orde reaksi terhadap OCl⁻ Orde reaksi terhadap OCl⁻ (i) dapat ditentukan dengan cara membandingkan laju reaksi ketiga dan keempat. Orde reaksi OCl⁻ adalah 1. (Hasil perhitungan terlampir dalam gambar). Persamaan laju reaksi dari reaksi di atas adalah sebagai berikut. I⁻(aq) + OCl⁻(aq) → IO⁻(aq) + Cl⁻(aq) V = k [I⁻]ⁿ[OCl⁻]ⁱ nilai n dan i adalah satu. Jadi hukum laju reaksi di atas adalah V = k [I⁻][OCl⁻].
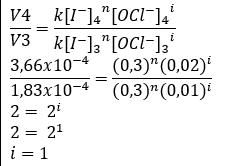
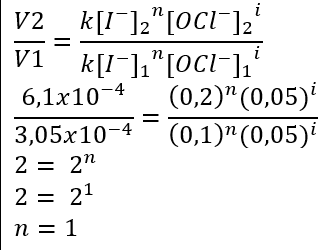
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



