OD
Olivia D
05 Juni 2022 05:35
Iklan
OD
Olivia D
05 Juni 2022 05:35
Pertanyaan
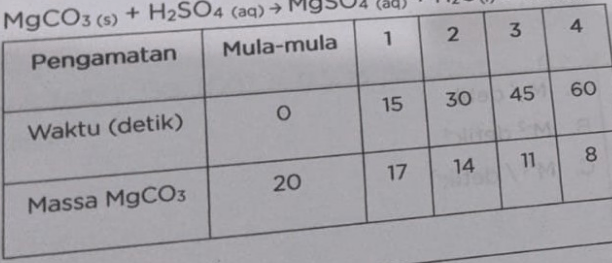
Perhatikan reaksi berikut : MgCO3 (s) + H2SO4 (aq) → MgSO4 (aq) + H2O + CO2(g) Tentukan berapa laju reaksi dari MgCO3 (Mr = 84 g/mol). A. 3 x 10^-2 mol/detik B. 2 x 10^-3 mol/detik C. 2 x 10^-2 mol/detik D. 3 x 10^-1 mol/detik E. 3 x 10^-3 mol/detik
3
1
Iklan
GP
G. Pramiyanti
05 Juni 2022 14:03
Jawaban terverifikasi
Laju reaksi dari MgCO3 adalah B. 2 x 10^-3 mol/detik. Pembahasan : Laju reaksi adalah perubahan jumlah zat tiap satuan waktu. Laju reaksi dapat dihitung menggunakan rumus : v = ∆mol / ∆t Dimana, v = laju reaksi (mol/detik) ∆mol = perubahan jumlah zat (mol) ∆t = perubahan waktu (detik) Dari tabel diperoleh data sebagai berikut : *∆ massa = 3 gram *Mr MgCO3 = 84 gram/mol Dari data tersebut dapat kita hitung ∆mol MgCO3. ∆mol MgCO3 = (∆massa/Mr) ∆mol MgCO3 = (3 gram/84 gram.mol-1) = 0,036 mol. * ∆t = 15 detik Sehingga v = (∆mol MgCO3/∆t) v= (0,036 mol/15 detik) = 2 x 10^-3 mol/detik. Dengan demikian laju reaksi dari MgCO3 adalah B. 2 x 10^-3 mol/detik.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



