IF
Ichsanul F
22 Juni 2022 16:00
Iklan
IF
Ichsanul F
22 Juni 2022 16:00
Pertanyaan
Perhatikan reaksi: aA + bB → Produk. Ketika konsentrasi kedua reaktan, A dan B dinaikkan dua kali lipat, laju reaksi meningkat menjadi 8 kali lipat. Namun, ketika konsentrasi A dinaikkan dua kali lipat sedangkan konsentrasi B tetap, laju reaksi meningkat menjadi dua kali lipat. Hukum laju reaksi tersebut (A) v = k [A]³ (B) v = k [A]²[B] (C) v = k [A][B]² (D) v = k [A][B] (E) tidak dapat ditentukan dari percobaan di atas
4
1
Iklan
NT
N. Tri
Mahasiswa/Alumni Universitas Sebelas Maret
22 Juni 2022 17:20
Jawaban terverifikasi
Jawaban yang benar adalah C Laju reaksi adalah laju berkurangnya konsentrasi zat pereaksi atau laju bertambahnya konsentrasi hasil reaksi untuk setiap satuan waktu. Perhatikan penjelasan pada gambar terlampir berikut ya Jadi, Hukum laju reaksi tersebut adalah v = k [A][B]²
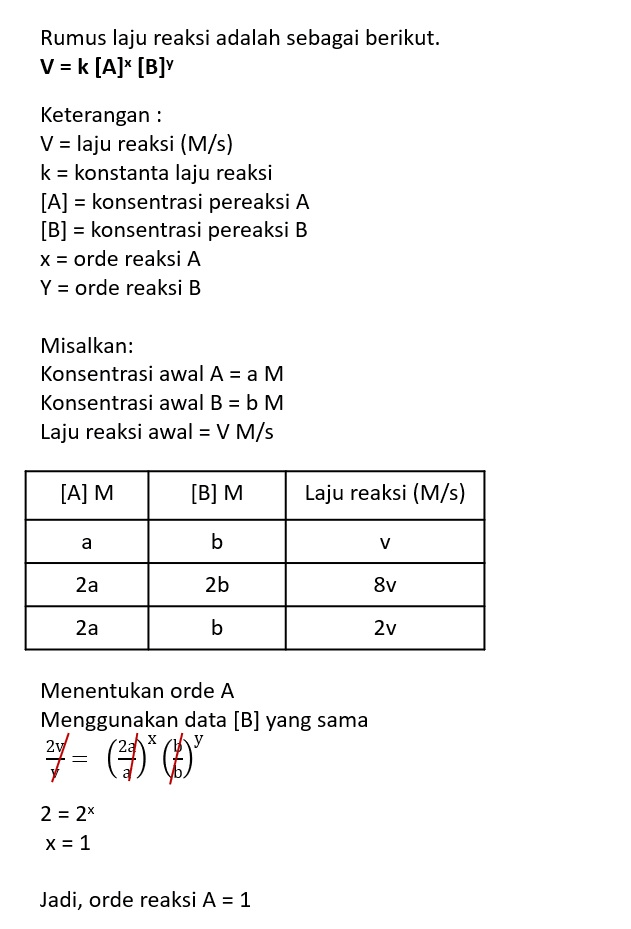

· 3.9 (13)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



