VN
Via N
29 Januari 2022 14:25
Iklan
VN
Via N
29 Januari 2022 14:25
Pertanyaan
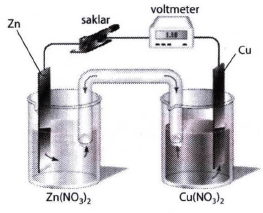
Perhatikan rangkaian sel Volta berikut. Jika diketahui potensial elektrode Zn dan Cu : Zn^2+(aq) + 2e → Zn(s) E° = −0,76 volt Cu^2+(aq) + 2e → Cu(s) E° = +0,34 volt Penulisan diagram sel yang paling tepat dari sel elektrokimia tersebut adalah ... a. Cu / Cu^2+ // Zn / Zn^2+ b. Zn / Zn^2+ // Cu^2+ / Cu c. Cu^2+ / Cu // Zn^2+ / Zn d. Zn^2+ / Zn // Cu / Cu^2+ e. Zn / Zn^2+ // Cu / Cu^2+
6
1
Iklan
WI
W. Imelda
Mahasiswa/Alumni Universitas Negeri Surabaya
08 Februari 2022 13:33
Jawaban terverifikasi
Hallo Via, kakak bantu jawab ya ^^ Jadi, jawaban yang benar untuk pertanyaan tersebut adalah Zn|Zn²⁺ || Cu²⁺|Cu (B). Ayo simak pembahasan berikut agar lebih paham ya ^^ Sel elektrokimia dibedakan menjadi dua yaitu: 1. Sel volta 2. Sel elektrolisis Sel volta merupakan reaksi redoks yang berjalan secara spontan dan selama reaksi berlangsung akan membebaskan energi listrik. Rangkaian pada sel volta yaitu terdiri dari elektrode, kabel listrik, larutan elektrolit, dan jembatan garam. Pada sel volta terdapat spesifikasi diantaranya: 1. Anoda, tempat oksidasi (bermuatan negatif). 2. Katoda, tempat reduksi (bermuatan positif). 3. Jembatan garam, penghubung daerah anode-katode, biasanya berfungsi sebagai penyeimbang ion-ion yang berlebihan. Di dalam sel volta ini juga terdapat deret volta, yaitu deret kereaktifan logam yang diurutkan berdasarkan besarnya potensial reduksi yang dimiliki. Berikut ini urutan logam pada deret volta: K - Ba - Ca - Na - Mg - Al - Mn - Zn - Cr - Fe - Cd - Co - Ni - Sn - Pb - [H] - Sb - Bi - Cu - Hg - Ag - Pt - Au Semakin ke kiri nilai potensial reduksi semakin kecil, logamnya sangat reaktif sehingga cenderung mengalami oksidasi. Sebaliknya semakin ke kanan, nilai potensial reduksi semakin besar, logam semakin inert sehingga cenderung mengalami reduksi. Potensial elektrode Zn dan Cu : Zn²⁺(aq) + 2e → Zn(s) E° = −0,76 volt Cu²⁺(aq) + 2e → Cu(s) E° = +0,34 volt Berdasarkan data tersebut, E° Zn lebih kecil dibandingkan dengan E° Cu, maka pada elektrode Zn terjadi reaksi oksidasi sedangkan elektrode Cu terjadi reaksi reduksi. Sehingga reaksinya yaitu: Red: Cu²⁺(aq) + 2e⁻ ➝ Cu(s) (katoda) Oks: Zn(s) ➝ Zn²⁺(aq) + 2e⁻ (anoda) -------------------------------------------------- + Rx total: Cu²⁺(aq) + Zn(s) ➝ Cu(s) + Zn²⁺(aq) Setelah reaksi total terbentuk, maka dapat diubah ke dalam bentuk notasi sel, adapun berikut ini beberapa aturan dalam penulisan notasi sel yaitu: 1. Reaksi yang terjadi pada anoda dituliskan terlebih dahulu (sisi kiri), kemudian diikuti reaksi yang terjadi pada katoda (sisi kanan). 2. Kedua sisi akan dipisahkan oleh dua buah garis. Dua garis ini menyatakan adanya rangkaian dalam dan luar pada saat reaksi. 3. Elektrode dituliskan diujung-ujung notasi sel, kemudian ada pemisah garis tunggal antara elektrode dengan larutan yang menyatakan perbedaan fasa. Sehingga, apabila berdasarkan aturan tersebut maka: Sisi kiri: Zn(s)|Zn²⁺(aq) Sisi kanan: Cu²⁺(aq)|Cu(s) Ketika digabungkan akan menjadi: Zn(s)|Zn²⁺(aq)||Cu²⁺(aq)|Cu(s)
· 5.0 (2)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



