Dtpm D
15 September 2022 13:22
Iklan
Dtpm D
15 September 2022 13:22
Pertanyaan
perhatikan diagram Hess berikut! manakah yang memenuhi Hukum Hess? a. ΔH1 + ΔH2 = ΔH3 + ΔH4 b. ΔH1 + ΔH3 = ΔH4 - ΔH2 c. ΔH1 = ΔH3 + ΔH4 - ΔH2 d. ΔH3 = ΔH2 = ΔH1 - ΔH4 e. ΔH3 - ΔH1 = ΔH2 - ΔH4
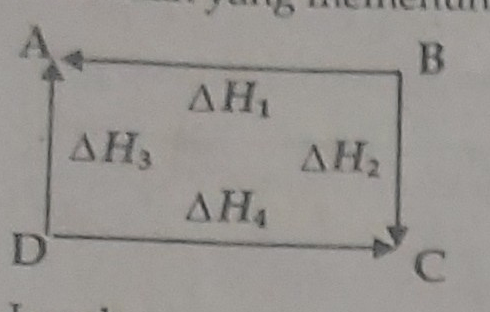
14
1
Iklan
L. Andini
24 November 2022 06:02
<p>Jawaban nya adalah ΔH1 + ΔH4 = ΔH2 + ΔH3 (tidak ada opsi yang sesuai)</p><p> </p><p>Perubahan entalpi dapat ditentukan dengan Hukum Hess, </p><p>Gerrmain Henry <strong>Hess</strong> menjelaskan bahwa : "Apabila sebuah reaksi berlangsung dalam dua tahap reaksi atau lebih, maka perubahan entalpi terhadap reaksi tersebut akan bernilai sama dengan jumlah perubahan entalpi dari seluruh tahapan yang terjadi."</p><p>Hal ini menjelaskan bahwa setiap reaksi kimia memiliki perubahan total entalpi yang tetap serta tidak tergantung pada tahapan reaksinya. </p><p>Perubahan entalpi reaksi dapat dihitung dari entalpi produk dan entalpi reaktan pembentuknya. </p><p>Dari grafik diatas, A dan C merupakan produk (spesi yang ditunjuk panah merupakan produk), sedangkan B dan D merupakan reaktan. </p><p>Perubahan entalpi dapat dituliskan dengan rumusan :</p><p>searah jarum jam = berlawanan jarum jam</p><p>Maka dari diagram tersebut, dapat diketahui rumus perubahan entalpi adalah :</p><p>ΔH1 + ΔH4 = ΔH2 + ΔH3</p>
Jawaban nya adalah ΔH1 + ΔH4 = ΔH2 + ΔH3 (tidak ada opsi yang sesuai)
Perubahan entalpi dapat ditentukan dengan Hukum Hess,
Gerrmain Henry Hess menjelaskan bahwa : "Apabila sebuah reaksi berlangsung dalam dua tahap reaksi atau lebih, maka perubahan entalpi terhadap reaksi tersebut akan bernilai sama dengan jumlah perubahan entalpi dari seluruh tahapan yang terjadi."
Hal ini menjelaskan bahwa setiap reaksi kimia memiliki perubahan total entalpi yang tetap serta tidak tergantung pada tahapan reaksinya.
Perubahan entalpi reaksi dapat dihitung dari entalpi produk dan entalpi reaktan pembentuknya.
Dari grafik diatas, A dan C merupakan produk (spesi yang ditunjuk panah merupakan produk), sedangkan B dan D merupakan reaktan.
Perubahan entalpi dapat dituliskan dengan rumusan :
searah jarum jam = berlawanan jarum jam
Maka dari diagram tersebut, dapat diketahui rumus perubahan entalpi adalah :
ΔH1 + ΔH4 = ΔH2 + ΔH3
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



