AM
Andi M
20 Mei 2022 10:53
Iklan
AM
Andi M
20 Mei 2022 10:53
Pertanyaan
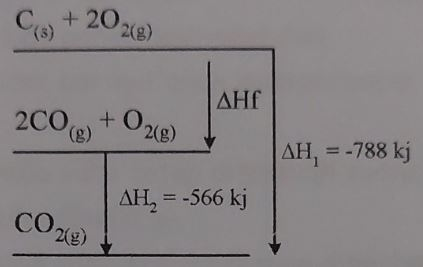
perhatikan diagram berikut! ΔHf COadalah ... .
6
1
Iklan
YY
Y. Yeni
Mahasiswa/Alumni Universitas Negeri Padang
21 Mei 2022 04:24
Jawaban terverifikasi
Jawaban ∆Hf CO = -111 kJ Perubahan entalpi ( ∆H ) adalah perpindahan kalor pada tekanan tetap. Menentukan perubahan entalpi suatu reaksi dapat menggunakan Hukum Hess yang menyatakan bahwa perubahan entalpi tidak tergantung pada berapa banyak tahapan reaksi, tetapi cuma bergantung pada keadaan awal dan akhir. Pada soal dapat di tentukan persamaan Hukum Hess ∆H1 = ∆Hf + ∆H2 -788 kJ = ∆Hf + (-566kJ ) -788 kJ + 566 kJ = ∆Hf -222 kJ = ∆Hf Persamaan termokimia dapat dituliskan 2C(s) + O₂(g) → 2CO(g) ∆Hf = -222 kJ Pada reaksi terbentuk 2 CO artinya 2 mol CO melepaskan energi -222 kJ. Perubahan entalpi standar ( ∆Hf ) adalah perubahan entalpi pembentukan satu mol senyawa dari unsur-unsurnya pada keadaan standar. Perubahan entalpi pembentukan standar 1 mol CO adalah -222 kJ / 2 mol = -111 kJ C(s) + 1/2 O₂(g) → CO(g) ∆Hf = -111 kJ Jadi dapat disimpulkan ∆Hf CO adalah -111 kJ.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



