NN
Najwa N
07 Februari 2022 16:10
Iklan
NN
Najwa N
07 Februari 2022 16:10
Pertanyaan
perhatikan beberapa molekul berikut! 1)AIF³ 2)NH³ 3)BF³ 4)H²O 5)CO² diantara molekul tersebut yg dapat bertindak sebagai basa lewis adalah
1
1
Iklan
AA
A. Anania
Mahasiswa/Alumni Hanyang University
18 Februari 2022 13:24
Jawaban terverifikasi
Hai Najwa, kakak akan coba bantu jawab pertanyaan kamu ya. Jawaban dari pertanyaan kamu adalah AlF3 (1), NH3 (2), dan H2O (4). Untuk dapat menjawab soal ini, kamu harus memahami konsep asam dan basa menurut Lewis ya. Menurut Lewis, yang dimaksud dengan asam adalah molekul yang dapat menerima pasangan elektron (electron acceptor), sedangkan basa adalah molekul yang dapat mendonorkan pasangan elektron (electron donor). Contohnya adalah: H+ + OH- → H2O H+ adalah molekul yang dapat menerima pasangan elektron dari OH-, sehingga merupakan asam Lewis. OH- adalah molekul yang dapat mendonorkan pasangan elektron untuk H+ dan membuat ikatan H-O-H, sehingga merupakan basa Lewis. Jika sudah jelas mengenai konsep asam-basa Lewis, kita cek satu persatu pilihan jawabannya ya. 1. AlF3. Al memiliki 5 elektron valensi. Pada struktur AlF3, Al menggunakan 3 elektron valensinya untuk berikatan dengan 3 atom F, sehingga masih tersisa 2 elektron bebas lagi (pasangan elektron bebas). Pasangan elektron ini dapat didonorkan kepada senyawa lain yang kekurangan elektron (senyawa elektrofil), sehingga AlF3 dapat disebut sebagai basa Lewis. 2. NH3. N memiliki 5 elektron valensi. Pada struktur NH3, N menggunakan 3 elektron valensinya untuk berikatan dengan 3 atom H, sehingga masih tersisa 2 elektron bebas lagi (pasangan elektron bebas). Pasangan elektron ini dapat didonorkan kepada senyawa lain yang kekurangan elektron (senyawa elektrofil), sehingga NH3 dapat disebut sebagai basa Lewis. 3. BF3. B memiliki 3 elektron valensi. Pada struktur BF3, B telah menggunakan 3 elektron valensinya untuk berikatan dengan 3 atom F, sehingga tidak ada sisa elektron lagi untuk didonorkan. Oleh karena itu, BF3 bukan basa Lewis. 4. H2O. O memiliki 6 elektron valensi. Pada struktur H2O, O menggunakan 2 elektron valensinya untuk berikatan dengan 2 atom H, sehingga masih tersisa 4 elektron bebas lagi (2 pasangan elektron bebas). Pasangan elektron ini dapat didonorkan kepada senyawa lain yang kekurangan elektron (senyawa elektrofil), sehingga H2O dapat disebut sebagai basa Lewis. 5. CO2. C memiliki 4 elektron valensi. Pada struktur CO2, C telah menggunakan 4 elektron valensinya untuk berikatan dengan 2 atom O, sehingga tidak ada sisa elektron lagi untuk didonorkan. Oleh karena itu, CO2 bukan basa Lewis. Untuk lebih jelasnya, kamu bisa melihat struktur Lewis nya pada gambar ya. Jadi, diantara molekul tersebut yg dapat bertindak sebagai basa Lewis adalah AlF3, NH3 dan H2O. Kakak harap penjelasan kakak dapat membantu kamu menyelesaikan soal ini ya. Tetap semangat! :)
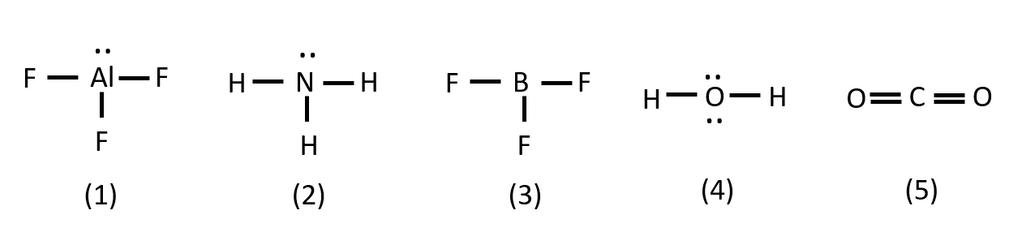
· 5.0 (1)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



