RE
Risnani E
12 November 2020 02:38
Iklan
RE
Risnani E
12 November 2020 02:38
Pertanyaan
MnO4- + C2O42- ---> MnO2 + CO2 ( suasana asam) ,setarakan dengan metode setengah reaksi!
195
4
Iklan
DA
D. Aprilia
Mahasiswa/Alumni Universitas Pendidikan Indonesia
01 Januari 2022 11:31
Jawaban terverifikasi
Halo, Risnani :) Jadi, persamaan reaksi setaranya dapat dilihat pada gambar dibawah yaaa. Agar lebih paham, yuk simak penjelasannya berikut ini! Kita tentukan dahulu biloks masing-masing unsur. MnO4– + C2O4^2– → MnO2 + CO2 biloks Mn pada MnO4– b.o Mn + (4×b.o O) = –1 b.o Mn + (4×(-2)) = –1 b.o Mn + (-8) = –1 b.o Mn = +7 biloks Mn pada MnO2 b.o Mn + (2×b.o O) = 0 b.o Mn + (2×(-2)) = 0 b.o Mn + (-4) = 0 b.o Mn = +4 Karena Mn mengalami perubahan biloks dari +7 menjadi +4 (biloks turun), maka reaksi yang dialami adalah reduksi. biloks C pada C2O4^2– : (2×b.o C) + (4×b.o O) = –2 (2×b.o C) + (4×(-2)) = –2 2×b.o C + (-8) = –2 2×b.o C = –2 + 8 b.o C = +6 /2 b.o C = +3 biloks C pada CO2 b.o C + (2×b.o O) = 0 b.o C + (2×(-2)) = 0 b.o C + (-4) = 0 b.o C = +4 Karena C mengalami perubahan biloks dari +3 menjadi +4 (biloks naik), maka reaksi yang dialami adalah oksidasi. Dalam metode setengah reaksi, langkah-langkah penyetaraan reaksinya yaitu : 1) Memisahkan setengah reaksi oksidasi dan setengah reaksi reduksi dari reaksi total. Reduksi = MnO4– → MnO2 Oksidasi = C2O4^2– → CO2 2) Menyetarakan jumlah atom yang mengalami perubahan bilangan oksidasi. Reduksi = MnO4– → MnO2 (Mn sudah sama, ada 1 di setiap ruas) Oksidasi = C2O4^2– → CO2 (C belum sama, di kiri ada 2 sedangkan di kanan baru 1), sehingga di ruas kanan (di senyawa CO2) tambahkan koefisien 2: Oksidasi = C2O4^2– → 2CO2 3) Menyetarakan jumlah oksigen pada masing-masing setengah reaksi. Pada suasana asam, menambahkan molekul H2O untuk setiap kekurangan satu atom oksigen pada ruas yang kekurangan atom O. Reduksi = MnO4– → MnO2 (jumlah O di kiri 4, di kanan 2, jadi di kanan tambahkan 2 molekul H2O) Reduksi = MnO4– → MnO2 + 2H2O Oksidasi = C2O4^2– → 2CO2 (jumlah O sudah sama di kedua ruas) 4) Menyetarakan jumlah hidrogen pada masing-masing setengah reaksi. Pada suasana asam, menyetarakan atom hidrogen dengan menambahkan ion H+ Reduksi = 4H+ + MnO4– → MnO2 + 2H2O 5) Menyetarakan muatan pada masing-masing setengah reaksi dengan menambahkan elektron pada ruas yang memiliki jumlah muatan lebih besar. Reduksi = 4H+ + MnO4– → MnO2 + 2H2O muatan kiri : +4 + (–1) = +3 muatan kanan : 0 sehingga di kiri ditambahkan 3 elektron : 3e- + 4H+ + MnO4– → MnO2 + 2H2O Oksidasi = C2O4^2– → 2CO2 muatan kiri : –2 muatan kanan : 0 sehingga di kanan ditambahkan 2e : C2O4^2– → 2CO2 + 2e- 6) Menyamakan jumlah elektron pada reaksi reduksi dan oksidasi dengan mengalikan jumlah elektron dengan koefisien tertentu. 3e- + 4H+ + MnO4– → MnO2 + 2H2O ⅼ×2ⅼ C2O4^2– → 2CO2 + 2e- ⅼ×3ⅼ sehingga menjadi, 6e- + 8H+ + 2MnO4– → 2MnO2 + 4H2O 3C2O4^2– → 6CO2 + 6e- 7) Menjumlahkan kedua persamaan setengah reaksi. 6e- + 8H+ + 2MnO4– → 2MnO2 + 4H2O 3C2O4^2– → 6CO2 + 6e- −−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−− 8H+ + 2MnO4– + 3C2O4^2– → 2MnO2 + 4H2O + 6CO2
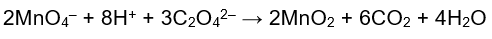
· 4.2 (20)
Iklan
RG
Rhendy G
28 November 2022 23:36
24%masa glukosa mr glukosa =180
· 0.0 (0)
AM
Asyifa M
05 Januari 2023 14:44
Setarakan reaksi redoks berikut (Point 30) MnO4- + C2O42- CO2 + MnO2 (suasana asam) Fe3+ + NH3OH+ Fe2+ + N2O (suasana basa)
· 5.0 (1)
MN
Molama N
21 Februari 2024 23:34
MnO₄⁻ + C₂O₄²⁻ ⇒ Mn²⁺ + CO₂ (Asam)
· 5.0 (1)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



