NC
Nabila C
11 Maret 2021 05:33
Iklan
NC
Nabila C
11 Maret 2021 05:33
Pertanyaan
larutan H2SO4 0,05 M mempunyai harga pH sebesar....
4
6
Iklan
IW
I. Wulandari
Mahasiswa/Alumni Universitas Sebelas Maret
05 Januari 2022 01:40
Jawaban terverifikasi
Halo Nabila, kakak bantu jawab yaa. Jawaban yang benar adalah 1. pH atau derajat keasaman digunakan untuk menyatakan tingkat keasaman atau kebasaan dari suatu larutan. Pada soal ini H2SO4 adalah larutan asam kuat dengan valensi 2 karena saat terionisasi menghasilkan 2H+. Maka untuk menghitung pH rumus nya adalah: pH = -log [H+] Terima kasih sudah bertanya, tetap gunakan Roboguru sebagai teman belajar mu yaa.
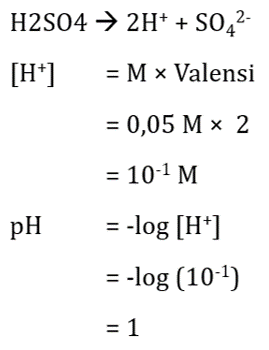
· 4.2 (5)
Iklan
AM
Andhini M
11 Maret 2021 10:43
H2SO4 -> 2H+ + SO42- karena H2SO4 termasuk asam kuat, maka konsentrasi H+ dapat dicari dengan rumus berikut. dengan x adalah banyaknya ion H+ dan Ma adalah molaritas asam. [H+]= x × Ma = 2 × 0,05 = 0,1 = 10 -¹ pH = - log [H+] = - log 10 -¹ = 1
· 4.7 (7)
MA
Mei A
14 Maret 2022 00:48
hitunglah pH larutan yang dibuat dengan melarutkan 4gram NaOH ke dalam 10liter air
· 0.0 (0)
HH
Hasan H
18 Januari 2023 06:53
hcooh 0,1m (ka =
· 0.0 (0)
HH
Hasan H
18 Januari 2023 06:54
hcooh 0,1m
· 0.0 (0)
TL
Tania L
04 Maret 2024 12:45
3. Tentukan pH larutan H2SO4 0,05 M (asam kuat)
· 0.0 (0)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



