Ichsanul F
22 Agustus 2022 23:44
Iklan
Ichsanul F
22 Agustus 2022 23:44
Pertanyaan
Jika unsur X dan Y bersenyawa, bentuk molekul senyawa yang terjadi adalah .... (A) jungkat-jungkit. (B) bentuk V. (C) piramida segitiga. (D) bujur sangkar. (E) segitiga planar.
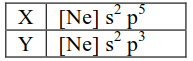
4
1
Iklan
A. Atikasari
Mahasiswa/Alumni Universitas Negeri Yogyakarta
11 Oktober 2022 12:12
<p>Jawaban yang tepat adalah opsi C.</p><p> </p><p>Penentuan bentuk molekul digunakan teori domain elektron atau Teori VSEPR. Bentuk molekul menyatakan suatu notasi yang digunakan pada suatu molekul yang menyatakan jumlah PEI (Pasangan elektron Ikatan) dan PEB (Pasangan Elektron Bebas) yang berada di sekitar atom pusat. Dalam teori VSEPR berlaku persamaan untuk penentuan bentuk suatu molekul, yaitu:<br>AXmEn <br>dimana, <br>A : atom pusat <br>X : PEI<br>m : jumlah PEI<br>E : PEB<br>n : jumlah PEB</p><p>• Konfigurasi unsur Y dan X<br>Y : [Ne] 3s² 3p³ (elektron valensi = 5, Y memerlukan 3 elektron agar stabil sesuai aturan oktet (8 elektron valensi))<br>X : [Ne] 3s² 3p⁵ (elektron valensi = 7, X memerlukan 1 elektron agar stabil sesuai aturan oktet (8 elektron valensi))</p><p>Unsur X dan Y dapat membentuk ikatan kovalen karena adanya pemakaian elektron bersama. Apabila senyawa yang terbentuk adalah YX₃, maka perhatikan struktur Lewis pada gambar.<br>PEI => 3<br>PEB => 1<br>Rumus bentuk molekul => AX₃E<br>Bentuk molekul => piramida trigonal atau piramida segitiga.</p><p> </p><p>Jadi, jika unsur X dan Y bersenyawa, bentuk molekul senyawa yang terjadi adalah piramida segitiga.</p>
Jawaban yang tepat adalah opsi C.
Penentuan bentuk molekul digunakan teori domain elektron atau Teori VSEPR. Bentuk molekul menyatakan suatu notasi yang digunakan pada suatu molekul yang menyatakan jumlah PEI (Pasangan elektron Ikatan) dan PEB (Pasangan Elektron Bebas) yang berada di sekitar atom pusat. Dalam teori VSEPR berlaku persamaan untuk penentuan bentuk suatu molekul, yaitu:
AXmEn
dimana,
A : atom pusat
X : PEI
m : jumlah PEI
E : PEB
n : jumlah PEB
• Konfigurasi unsur Y dan X
Y : [Ne] 3s² 3p³ (elektron valensi = 5, Y memerlukan 3 elektron agar stabil sesuai aturan oktet (8 elektron valensi))
X : [Ne] 3s² 3p⁵ (elektron valensi = 7, X memerlukan 1 elektron agar stabil sesuai aturan oktet (8 elektron valensi))
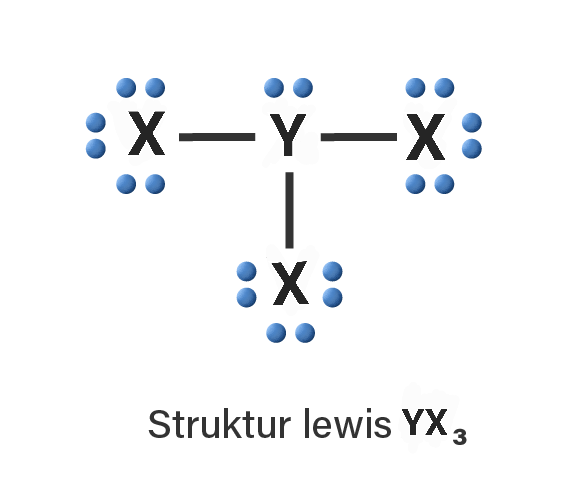
Unsur X dan Y dapat membentuk ikatan kovalen karena adanya pemakaian elektron bersama. Apabila senyawa yang terbentuk adalah YX₃, maka perhatikan struktur Lewis pada gambar.
PEI => 3
PEB => 1
Rumus bentuk molekul => AX₃E
Bentuk molekul => piramida trigonal atau piramida segitiga.
Jadi, jika unsur X dan Y bersenyawa, bentuk molekul senyawa yang terjadi adalah piramida segitiga.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



