SA
Syifa A

30 Juli 2023 13:05
Iklan
SA
Syifa A

30 Juli 2023 13:05
Pertanyaan
Jika kulit K hanya mempunyai subkulit 1s, kulit L mempunyai subkulit 2s dan 2p. kulit M mempunyai subkulit 3s, 3p, dan 3d, maka berapa elektron paling banyak yang akan menempati kulit K. L. dan M? Bandingkan dengan konfigurasi elektron pada teori atom Bohr
Jika kulit K hanya mempunyai subkulit 1s, kulit L mempunyai subkulit 2s dan 2p. kulit M mempunyai subkulit 3s, 3p, dan 3d, maka berapa elektron paling banyak yang akan menempati kulit K. L. dan M? Bandingkan dengan konfigurasi elektron pada teori atom Bohr
1
1
Iklan
JS
J. Siregar
Mahasiswa/Alumni Universitas Negeri Medan
31 Juli 2023 02:27
Jawaban terverifikasi
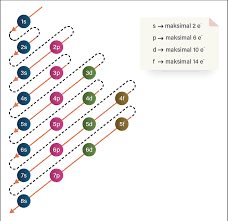
Jawaban yang benar adalah kulit K = 2 elektron; kulit L = 8 elektron; dan kulit M = 18 elektron. Konfigurasi elektron menunjukkan susunan elektron dalam suatu atom. Dalam penulisan konfigurasi elektron dapat menggunakan aturan Bohr (berdasarkan kulit) maupunn asas Aufbau (berdasarkan subkulit). 1) Penulisan konfigurasi elektron dapat kita tinjau berdasarkan kulit. Kulit atom dimulai dari yang paling dekat dengan inti atom yaitu kulit K, L, M, N, dan seterusnya dengan urutan kulit-1, kulit-2, kulit-3, kulit-4. Nomor kulit bisa kita simbolkan dengan n. Oleh karena itu, untuk menentukan jumlah setiap elektron dalam atom berlaku persamaan 2n². Jumlah maksimal elektron pada setiap masing-masing kulit sebagai berikut: • K (n=1), jumlah elektron = 2(1)² = 2 elektron • L (n=2), jumlah elektron = 2(2)² = 8 elektron • M (n=3), jumlah elektron = 2(3)² = 18 elektron • N (n=4), jumlah elektron = 2(4)² = 32 elektron 2) Penulisan konfigurasi elektron berdasarkan subkulit (tingkat energi) sesuai aturan Aufbau. Setiap kulit memiliki subkulit sebagai berikut. • Kulit K memiliki 1 subkulit yaitu 1s. • Kulit L memiliki 2 subkulit yaitu 2s dan 2p. • Kulit M memiliki 3 subkulit yaitu 3s, 3p, dan 3d. • dst. Setiap subkulit juga memiliki jumlah elekton maksimal. • subkulit s menampung maksimal 2 elektron. • subkulit p menampung maksimal 6 elektron. • subkulit d menampung maksimal 10 elektron. Jika kita buat hubungan antara kulit, subkulit dan jumlah maksimalkan elektron maka: • Kulit K, subkulit 1s = 2 elektron. • Kulit L, subkulit 2s = 2 elektron dan subkulit 2p = 6 elektron, dengan total sebanyak 8 elektron. • Kulit M, subkulit 3s = 2 elektron, subkulit 3p = 6 elektron, dan subkulit 3d = 10 elektron dengan total sebanyak 18 elektron. Dengan demikian, jumlah maksimal elekton dalam setiap kulit adalah kulit K = 2 elektron; kulit L = 8 elektron; dan kulit M = 18 elektron.
· 5.0 (2)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



