AA
Ana A
24 April 2022 03:52
Iklan
AA
Ana A
24 April 2022 03:52
Pertanyaan
Jika diketahui nomor atom H=1,Be=4,B =5,C=6,N=7,O=8,Cl=17, pasangan yang tepat antara rumus molekul, bentuk molekul dan jenis kemolaran ikatannya adalah ....
5
1
Iklan
YA
Y. Ayu
25 April 2022 00:45
Jawaban terverifikasi
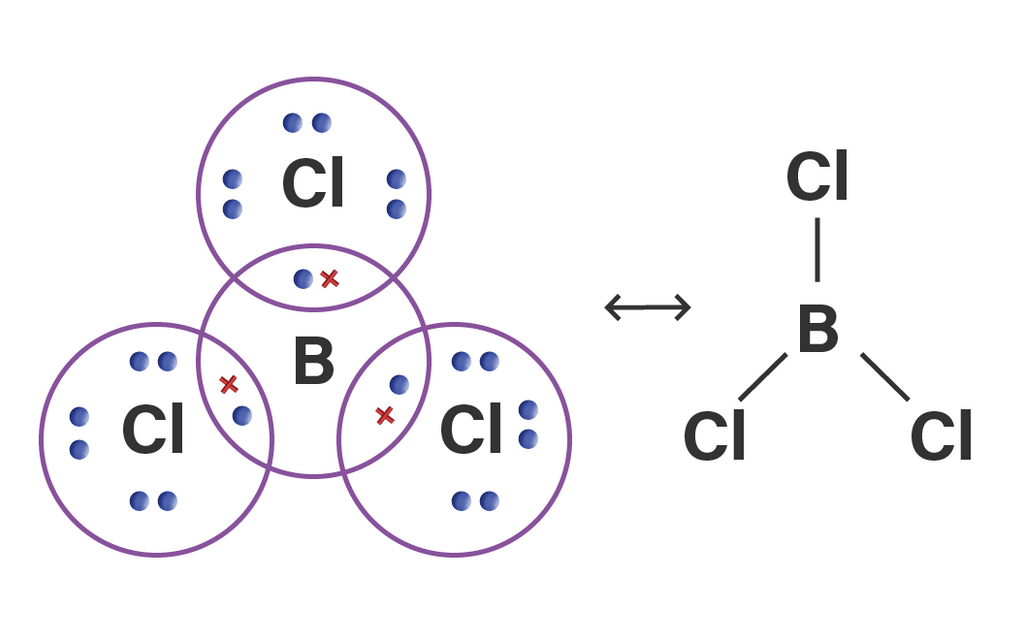
Hai Ana, kakak bantu jawab pertanyaanmu ya. Jawaban: A. BCl3 dengan bentuk molekul trigonal planar dan bersifat non polar Elektron valensi B dan Cl dapat diketahui dari konfigurasi elektronnya. 5B = 2 3 ⇒ elektron valensi = 3 17Cl = 2 8 7 ⇒ elektron valensi = 7 Untuk mencapai kestabilan atom B membutuhkan 3 elektron karena terjadi penyimpangan kaidah oktet. Kaidah oktet merupakan aturan agar suatu atom dikelilingi 8 elektron saat berikatan dengan atom lain. Sedangkan untuk atom B pada BCl3 hanya dikelilingi oleh 6 elektron. PEI adalah pasangan elektron ikatan yang mana digunakan berikatan bersama elektron valensi atom lain. Sedangkan PEB adalah pasangan elektron bebas yang tidak digunakan berikatan. PEB = ½(elektron valensi - elektron ikatan) PEB = ½(6 - 6) = 0 PEB Teori domain elektron adalah teori yang menyatakan bahwa pasangan elektron ikatan (PEI) dan pasangan elektron bebas (PEB) saling tolak-menolak. Teori ini dapat digunakan untuk memprediksi bentuk molekul. Untuk menentukan bentuk molekul menggunakan teori domain elektron, kamu bisa mengacu pada notasi VSEPR berikut: AXnEm A: atom pusat X: pasangan elektron ikatan (PEI) n: jumlah PEI dalam molekul E: pasangan elektron bebas (PEB) m: jumlah PEB dalam molekul Notasi VSEPR dari BCl3 adalah AX3. Jadi, bentuk molekulnya adalah trigonal planar. Bentuk molekul dan struktur Lewis BCl3 dapat dilihat pada gambar di lampiran. Senyawa kovalen polar adalah senyawa yang memiliki ikatan kovalen polar. Ikatan kovalen polar adalah ikatan yang pasangan elektron ikatannya cenderung tertarik ke salah satu atom yang berikatan. Ikatan kovalen polar terbentuk antara atom-atom unsur yang memiliki perbedaan nilai keelektronegatifan yang relatif besar. Sedangkan senyawa kovalen non polar adalah senyawa yang unsur-unsurnya berikatan kovalen dan mempunyai nilai elektronegatifitas yang sama atau hampir sama. Ciri senyawa polar sebagai berikut : -Memiliki kutub positif di satu sisi dan kutub negatif disisi lain. -Memiliki perbedaan keelektronegatifan yang besar antaratom berikatan. -Dapat larut dalam air dan pelarut polar. -Memiliki momen dipol > 1. -Bentuknya molekul tidak simetris. Ciri senyawa non polar sebagai berikut : -Tidak memiliki kutub -Perbedaan keelektronegatifan atom-atom berikatan relatif kecil. -Senyawanya mudah larut dalam pelarut nonpolar. -Memiliki momen dipol = 0. -Bentuk molekul simetris BCl3 tidak memiliki PEB dan berbentuk simetris, maka BCl3 bersifat nonpolar. Jadi, pasangan yang tepat antara rumus molekul, bentuk molekul dan jenis kemolaran ikatannya adalah BCl3 yang berbentuk trigonal planar dan bersifat non polar.
· 4.8 (4)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



