AC
Allisa C
31 Maret 2022 02:07
Iklan
AC
Allisa C
31 Maret 2022 02:07
Pertanyaan
Jika 54 g logam aluminium direaksikan dengan 48 g oksigen sehingga menghasilkan senyawa aiuminium oksida (Al₂O₃). Tentukan berapa massa senyawa aluminium oksida yang terbentuk!
13
1
Iklan
YA
Y. Ayu
31 Maret 2022 12:29
Jawaban terverifikasi
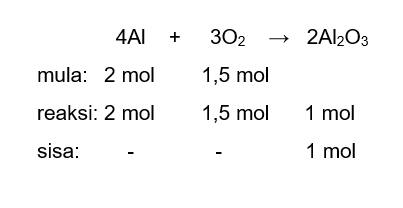
Hai Allisa, kakak bantu jawab pertanyaanmu ya. Jawaban: Massa Al2O3 yang terbentuk sebanyak 102 gram Reaksi antara logam Al dan oksigen: 4Al + 3O2 → 2Al2O3 Untuk menentukan zat yang bereaksi dan bersisa, perlu ditentukan mol masing-masing pereaksi. n = m/Mr Ar Al = 27 g/mol Mr O2 = 2 x Ar O = 2 x 16 g/mol = 32 g/mol n Al = 54 g/27 g/mol = 2 mol n O2 = 48 g/32 g/mol = 1,5 mol Perbandingan mol sebanding dengan perbandingan koefisien reaksinya. Maka, persamaan reaksi beserta mol yang terlibat dapat dilihat pada gambar di lampiran. Mol Al2O3 yang terbentuk sebanyak 1 mol. Massa Al2O3 sebanyak: m = n x Mr Mr Al2O3 = 2 x Ar Al + 3 x Ar O Mr Al2O3 = 2 x 27 g/mol + 3 x 16 g/mol Mr Al2O3 = 102 g/mol m Al2O3 = 1 mol x 102 g/mol = 102 g
· 5.0 (1)
JA
JACKLAND A
14 April 2023 06:26
Thk
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



