VN
Via N
19 Februari 2022 08:36
Iklan
VN
Via N
19 Februari 2022 08:36
Pertanyaan
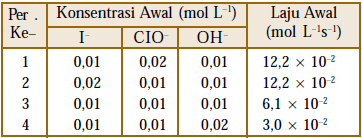
Ion iodida dioksidasi menjadi ion hipoiodit (IO^–) dengan ion hipoklorit (ClO^–) dalam larutan basa. Persamaan kimianya: I^– (aq) + ClO^– (aq) → IO^– (aq) + Cl– (aq) Dengan data sebagai berikut: Tentukan hukum laju untuk reaksi tersebut dan tentukan nilai tetapan lajunya.
2
1
Iklan
YY
Y. Yosua
21 Februari 2022 12:56
Jawaban terverifikasi
Halo Via, kakak bantu jawab ya :) Jawaban : v = 6,1[Cl^-][ClO^-][OH^-]^-1 M/s Laju reaksi adalah laju yang diperlukan suatu senyawa untuk bereaksi (Reaktan mengalami pengurangan komposisi, sedangkan produk mengalami pertambahan komposisi). Laju reaksi sebanding dengan konsentrasi reaktan dengan ordenya masing-masing. Misalkan dimiliki reaksi : A + B => C + D Maka laju reaksinya dirumuskan dalam v = k[A]^m[B]^n Dengan : k = konstanta laju reaksi [A] = konsentrasi senyawa A [B] = konsentrasi senyawa B m = orde terhadap senyawa A n = orde terhadap senyawa B Dalam menentukan nilai k, m, dan n dapat dilakukan dengan langkah-langkah berikut : 1. Bandingkan data percobaan untuk memperoleh nilai m dan n 2. Substitusikan nilai m dan n pada salah satu data untuk mendapat nilai k Terdapat tiga senyawa pada reaktan sehingga persamaan reaksi yang mungkin adalah v = k[A]^m[B]^n[C]^p. Ditentukan nilai m,n,p sebagai berikut : Bandingkan data ke (2) dan (3) sehingga diperoleh : k(0,02)^m.(0,01)^n.(0,01)^p = 12,2.10^-2 k(0,01)^m.(0,01)^n.(0,01)^p = 6,1.10^-2 ___________________________ : 2^m = 2 m = 1 Bandingkan persamaan ke (1) dan (3) sehingga diperoleh : k(0,01)^m.(0,02)^n.(0,01)^p = 12,2.10^-2 k(0,01)^m.(0,01)^n.(0,01)^p = 6,1.10^-2 ___________________________ : 2^n = 2 n = 1 Bandingkan persamaan ke (3) dan (4) sehingga diperoleh : k(0,01)^m.(0,01)^n.(0,01)^p = 6,1.10^-2 k(0,01)^m.(0,01)^n.(0,02)^p = 3,0.10^-2 ___________________________ : (1/2)^p = 2^1 2^-p = 2^1 p = -1 Sehingga diperoleh persamaan reaksi sementara adalah v = k[Cl^-][ClO^-][OH^-]^-1. Substitusikan data (1) ke dalam percobaan diperoleh : v = k[Cl^-][ClO^-][OH^-]^-1 12,2.10^-2 M/s = k.(0,01 M).(0,02 M).(0,01 M)^-1 k = 6,1/s Dengan demikian, persamaan reaksinya adalah v = 6,1[Cl^-][ClO^-][OH^-]^-1 M/s.
· 5.0 (1)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



