IP
Intan P
24 Mei 2022 08:03
Iklan
IP
Intan P
24 Mei 2022 08:03
Pertanyaan
Hitunglah volume dari larutan HNO3 yang harus ditambahkan dalam 100mL larutan NH3 0,1M untuk menghasilkan larutan penyangga dengan PH 9(Kb:10^-5)
3
1
Iklan
MB
M. Bimba
25 Mei 2022 01:54
Jawaban terverifikasi
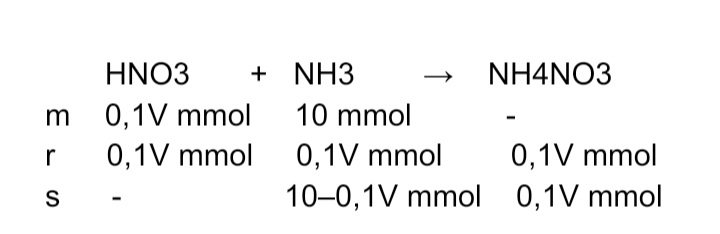
Jawaban: 50 mL Larutan penyangga adalah larutan yang dapat mempertahankan pH dengan menambah sedikit asam, basa, atau air. Larutan asam nitrat (HNO3) ialah asam kuat, sedangkan larutan amonia NH3 ialah basa lemah. Campuran larutan antara asam kuat dan basa lemah akan menghasilkan larutan penyangga yang bersifat basa. Maka, untuk menentukan volume HNO3 yang dibutuhkan tahapan yang dilakukan sebagai berikut: 1. Menentukan mol sisa Apabila molaritan HNO3 dianggap 0,1 M, maka: Mol HNO3 = M × V Mol HNO3 = 0,1 M × V mL Mol HNO3 = 0,1V mmol Mol NH3 = M × V Mol NH3 = 0,1 M × 100 mL Mol NH3 = 10 mmol Reaksi yang terjadi dan perhitungan MRS dapat dilihat pada gambar (terlampir). Berdasarkan reaksi tersebut, mol NH3 pada akhir reaksi bersisa, maka penyangga bersifat basa. 2. Menentukan konsentrasi OH- pH = 14 – pOH pOH = 14 – 9 pOH = 5 [OH-] = 10^-5 M 3. Menentukan nilai V Berdasarkan reaksi pada gambar, garam NH4NO3 akan mengion menghasilkan ion NH4+ (asam konjugasi), seperti reaksi berikut: NH4NO3 → NH4+ (aq) + NO3- (aq) Karena koefisien garam dan asam konjugasi sama, maka jumlah molnya juga sama. Maka: [OH-] = Kb × (mol basa lemah : mol asam konjugasi) 10^-5 M = 10^-5 × (10–0,1V mmol : 0,1V mmol) 10^-5 M : 10^-5 = 10–0,1V mmol : 0,1V mmol 1 = 10–0,1V mmol : 0,1V mmol 0,1V = 10 – 0,1V 0,1V + 0,1V = 10 0,2V = 10 V = 10 : 0,2 V = 50 4. Menentukan volume HNO3 Mol HNO3 = 0,1V mmol Mol HNO3 = 0,1 × 50 mmol Mol HNO3 = 5 mmol Apabila konsentrasi HNO3 dianggap = 0,1 M, maka Mol HNO3 = M × V V = Mol HNO3 : M V = 5 mmol : 0,1 M V = 50 mL Jadi, volumw HNO3 yang dibutuhkan adalah 50 mL.
· 5.0 (1)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



