DA
Dwi A
30 April 2020 14:28
Iklan
DA
Dwi A
30 April 2020 14:28
Pertanyaan
Hitung ph campuran jika 100 ml larutan NH3 (kb NH3 = 10 pangkat min 5) 0, 4 M dengan 50 mL larutan H2 SO4 0,1 M
3
1
Iklan
CY
C. Yudha
Mahasiswa/Alumni Politeknik Negeri Bandung
28 Desember 2021 14:04
Jawaban terverifikasi
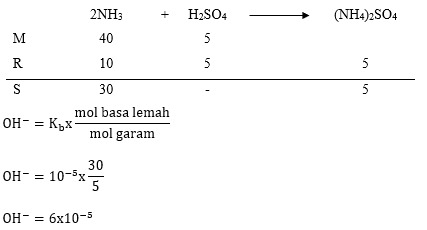
Halo Dwi, jawaban dari pertanyaan tersebut adalah 9+log 6 atau 9,778. Ayo simak pembahasan berikut agar kamu lebih paham ya^_^ NH3 merupakan basa lemah, H2SO4 merupakan asam kuat. Campuran basa lemah dan basa kuat dapat menghasilkan larutan penyangga. Larutan penyangga adalah larutan yang dapat mempertahankan harga pH ketika ditambah sedikit asam, basa dan dilakukan pengenceran dengan catatan zat yang lemah harus bersisa dan zat yang kuat harus habis bereaksi. Untuk menjawab soal ini harus menentukan masing-masing mol zat yang terlibat. mol NH3=volume NH3 x molaritas NH3 mol NH3=100 mL x 0,4 mol/L mol NH3=40 mmol mol H2SO4=volume H2SO43 x molaritas H2SO4 mol H2SO4=50 mL x 0,1 mol/L mol H2SO4=5 mmol Kemudian lakukan penulisan persamaan reaksi dan menghitung pH. Dengan mengacu ke perhitungan yang terlampir maka pOH=-log [OH-] pOH=-log 6x10^-5 pOH=5-log 6 pH+pOH=14 pH=14-pOH pH=14-(5-log 6) pH=9+log 6 log 6=0,778 pH=9,778
· 4.0 (5)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



