Labiibah T
12 September 2023 05:33
Iklan
Labiibah T
12 September 2023 05:33
Pertanyaan
halo kak! ada yg bisa bantu aku ga ya secepatnya??? dan serta pengertian nya?? terimakasih 🙏😄
halo kak! ada yg bisa bantu aku ga ya secepatnya??? dan serta pengertian nya?? terimakasih 🙏😄
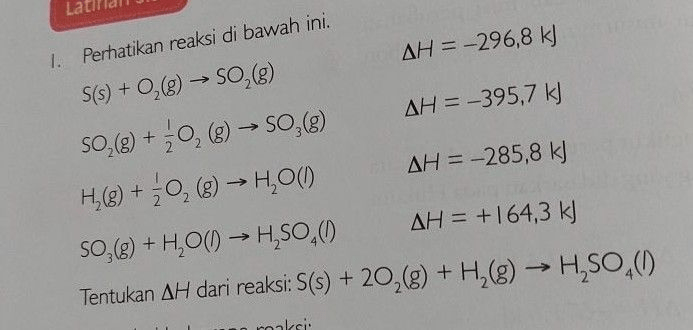
1
2
Iklan
Tjendana T

Community
12 September 2023 06:09
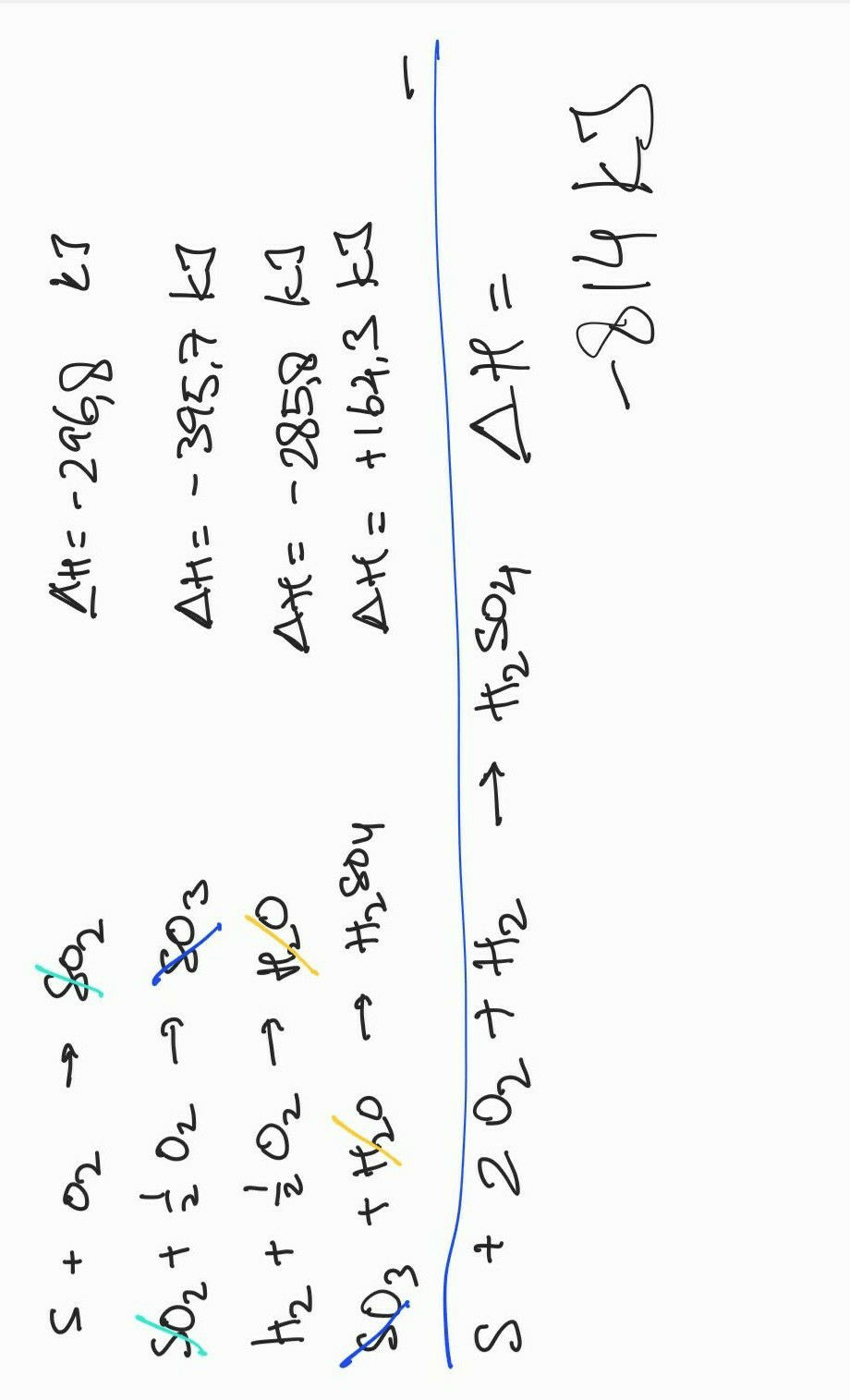
<p><strong>Pembahasan </strong></p><p> </p><p>Diketahui entalpi pembentukan dari masing2 reaksi, yg ditanyakan entalpi pembentukan H2SO4.... </p><p>Tinggal dijumlahkan saja, lihat caranya pd foto terlampir. </p><p> </p><p>Jawaban <strong>-814 kJ/mol</strong></p>
Pembahasan
Diketahui entalpi pembentukan dari masing2 reaksi, yg ditanyakan entalpi pembentukan H2SO4....
Tinggal dijumlahkan saja, lihat caranya pd foto terlampir.
Jawaban -814 kJ/mol
· 5.0 (1)
Iklan
Sahel S
13 September 2023 02:03
<p>Untuk menentukan ΔH dari reaksi: S (s) + 2 O2 (g) + H2 (g) → H2SO4 (l), kita dapat menggunakan Hukum Hess. Hukum Hess menyatakan bahwa perubahan entalpi suatu reaksi tidak berubah meskipun reaksi tersebut berasal dari beberapa langkah.</p><p>Berikut adalah langkah-langkah untuk menyelesaikan masalah ini:</p><p>1. Pertama, kita lihat reaksi yang diberikan dan entalpi masing-masing reaksi:</p><p>S (s) + O2 (g) → SO2 (g) ΔH = -296,8 kJ<br>SO2 (g) + ½ O2 (g) → SO3 (g) ΔH = -395,7 kJ<br>H2 (g) + ½ O2 (g) → H2O (l) ΔH = -285,8 kJ<br>SO3 (g) + H2O (l) → H2SO4 (l) ΔH = +164,3 kJ</p><p>2. Kita dapat menjumlahkan semua reaksi tersebut untuk mendapatkan reaksi total yang kita inginkan:</p><p>S (s) + 2 O2 (g) + H2 (g) → H2SO4 (l)</p><p>3. Selanjutnya, kita menjumlahkan semua entalpi reaksi untuk mendapatkan ΔH total:</p><p>ΔH reaksi = -296,8 kJ + (-395,7 kJ) + (-285,8 kJ) + 164,3 kJ = -814 kJ</p><p>Jadi, ΔH untuk reaksi S (s) + 2 O2 (g) + H2 (g) → H2SO4 (l) adalah -814 kJ.</p>
Untuk menentukan ΔH dari reaksi: S (s) + 2 O2 (g) + H2 (g) → H2SO4 (l), kita dapat menggunakan Hukum Hess. Hukum Hess menyatakan bahwa perubahan entalpi suatu reaksi tidak berubah meskipun reaksi tersebut berasal dari beberapa langkah.
Berikut adalah langkah-langkah untuk menyelesaikan masalah ini:
1. Pertama, kita lihat reaksi yang diberikan dan entalpi masing-masing reaksi:
S (s) + O2 (g) → SO2 (g) ΔH = -296,8 kJ
SO2 (g) + ½ O2 (g) → SO3 (g) ΔH = -395,7 kJ
H2 (g) + ½ O2 (g) → H2O (l) ΔH = -285,8 kJ
SO3 (g) + H2O (l) → H2SO4 (l) ΔH = +164,3 kJ
2. Kita dapat menjumlahkan semua reaksi tersebut untuk mendapatkan reaksi total yang kita inginkan:
S (s) + 2 O2 (g) + H2 (g) → H2SO4 (l)
3. Selanjutnya, kita menjumlahkan semua entalpi reaksi untuk mendapatkan ΔH total:
ΔH reaksi = -296,8 kJ + (-395,7 kJ) + (-285,8 kJ) + 164,3 kJ = -814 kJ
Jadi, ΔH untuk reaksi S (s) + 2 O2 (g) + H2 (g) → H2SO4 (l) adalah -814 kJ.
· 5.0 (1)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



