OD
Olivia D
31 Maret 2022 07:34
Iklan
OD
Olivia D
31 Maret 2022 07:34
Pertanyaan
Fluorit (juga disebut fluor-tiang kapal) adalah suatu mineral yang terdiri atas kalsium fluorida, CaF2. Fluorit mempunyai warna bening atau putih, warna ungu, biru kehijau-hijauan, kuning kecoklatan, merah muda, atau merah. Fluorit juga mempunyai kekerasan pada skala 4, berat jenis 3,18 g/mL dengan kilau seperti kaca dan belahannya yang sempurna, mempunyai daya larut sedikit di dalam air. Fluorit memiliki berbagai macam kegunaan. Penggunaan utama adalah dalam metalurgi, keramik dan industri kimia, optik, dan lain-lain. Fluorspar adalah nama yang digunakan untuk perdagangan atau dalam bentuk olahan. Dijual dalam tiga kelas yang berbeda (asam, keramik dan metalurgi). 100 gram fluorin mengandung 51,282 gram unsur kalsium, dan 48,717 gram unsur fluor. Bila inti atom kalsium (massa molar 40,078 = 40) mengandung 20 neutron dan inti atom fluor (massa molar 18,998 = 19) mengandung 10 neutron, maka nilai keempat bilangan kuantum elektron terakhir atom fluor adalah ... (sumber: htps://id.wikimedia.ors/viki/fluorin) a. n = 2, l = 0, m = 0, s = +1/2 b. n = 2, l = 1, m = 0, s = -1/2 c. n = 2, l = 1, m = 1, s = +1/2 d. n = 2, l = 2, m = 1, s = +1/2 e. n = 2, l = 1, m = 1, s = -1/2
1
1
Iklan
AA
A. Atikasari
Mahasiswa/Alumni Universitas Negeri Yogyakarta
01 April 2022 03:23
Jawaban terverifikasi
Halo Olivia, kakak bantu jawab yaa Jawaban: B. Yuk simak penjelasan berikut, agar kamu lebih paham yaa ^^ Bilangan kuantum adalah bilangan yang menggambarkan kedudukan suatu elektron dalam model atom mekanika kuatum yang dicetuskan oleh Erwin Schrodinger. Terdapat 4 bilangan kuantum, antara lain: 1.Bilangan Kuantum Utama (n), menyatakan nomor kulit tempat elektron berada. 2.Bilangan Kuantum Azimuth (l), menyatakan jenis subkulit tempat elektron itu berada. Jenis subkulit terdiri atas s, p,d dan f. Besarnya bilangan kuantum azimuth (l) adalah 0 sampai dengan (n – 1) -> s (l = 0), p (l = 1), d (l = 2), f (l = 3). 3.Bilangan Kuantum Magnetik (m), menyatakan orbital khusus tempat elektron itu berada serta orientasi orbital dalam ruangan relatif terhadap inti. Subkulit s, maka nilai m = 0 Subkulit p, maka nilai m = -1, 0, +1 Subkulit d, maka nilai m = -2, -1, 0, +1, +2 Subkulit f, maka nilai m = -3, -2, -1, 0, +1, +2, +3 4.Bilangan kuantum Spin (s), menunjukkan arah rotasi suatu elektron dalam orbitnya dan dinyatakan dengan tanda panah, s = +1/2 jika orbital hanya terisi satu elektron saja atau arah panah ke atas, s = -1/2 jika orbital terisi penuh elektron berpasangan atau arah panah terakhir ke bawah. Atom fluor (F) mempunyai nomor massa 19 dan jumlah neutron 10, sehingga jumlah elektronnya sesuai dengan nomor atomnya (karena yang ditanyakan atom fluor, maka fluor dalam kondisi netral), Nomor atom F = jumlah elektron F = nomor massa - neutron = 19 - 10 = 9 >> Bilangan kuantum ₉F, yaitu: Konfigurasi elektron ₉F = 1s² 2s² 2p⁵ Elektron terakhirnya adalah 2p⁵. Bilangan kuantum ditentukan oleh elektron terakhir 2p⁵. Kulit 2, maka bilangan kuantum utama (n) = 2 Sub kulit p -> maka bilangan kuantum azimuth (l) = 1 Pada orbital p⁵ (terlampir pada gambar) elektron terakhir berhenti pada bilangan kuantum magnetik (m) = 0. elektron terakhir berhenti pada posisi ↓ , maka bilangan kuantum spin (s) = - 1/2 • Bilangan kuantum ₉F adalah n = 2, l = 1, m = 0, s = -1/2.
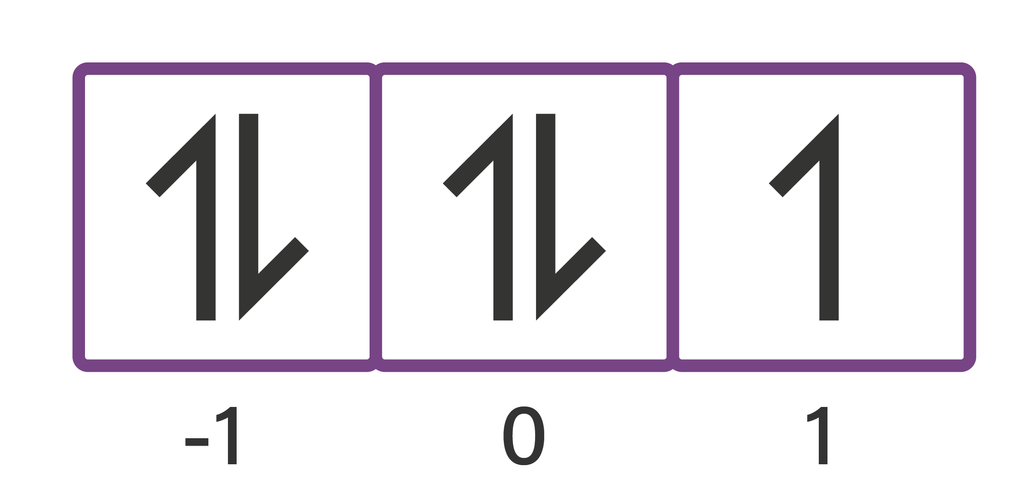
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



