AC
Allisa C
13 Maret 2022 14:45
Iklan
AC
Allisa C
13 Maret 2022 14:45
Pertanyaan
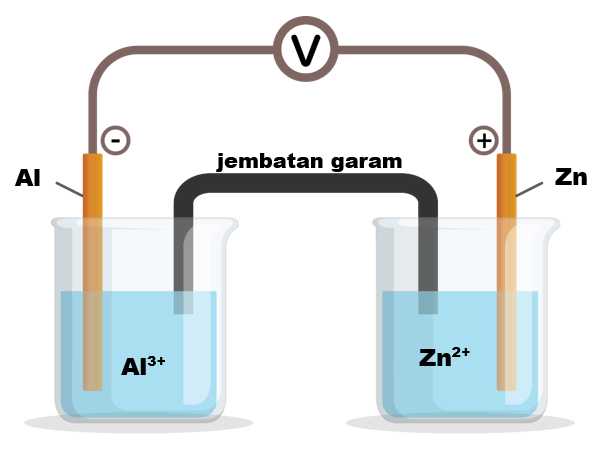
Diketahui: Zn²⁺(aq) + 2e⁻ ⇌ Zn(s) E° = -0,76 volt Al³⁺(aq) + 3e⁻ ⇌ Al(s) E° = -1,66 volt Lengkapi gambar sel berikut sesuai dengan data. Reaksi pada katode dan anode
5
1
Iklan
YA
Y. Ayu
25 Maret 2022 15:44
Jawaban terverifikasi
Hai Allisa, kakak bantu jawab pertanyaanmu ya. Jawaban: Rangkaian sel volta dapat dilihat pada gambar di lampiran. Reaksi anoda dan katoda: Katoda: 3Zn²⁺(aq) + 6e⁻ ⇌ 3Zn(s) | E° = -0,76 volt Anoda: 2Al(s) ⇌ 2Al³⁺(aq) + 6e⁻ | E° = -1,66 volt Reaksi sel: 2Al(s) + 3Zn²⁺(aq) ⇌ 2Al³⁺(aq) + 3Zn(s) | E° = +0,90 V Diagram sel adalah susunan sel volta antara anoda dan katoda. Katoda pada sel volta merupakan kutub positif dan mengalami reduksi sementara anoda merupakan kutub negatif dan mengalami oksidasi. Pada sel volta, reaksi dapat berlangsung spontan jika E°sel bernilai positif. Zat yang mengalami oksidasi dan reduksi dalam sel Volta dapat ditentukan berdasarkan harga potensial reduksi standarnya atau berdasarkan posisinya dalam deret Volta. E°sel = E° reduksi-E° oksidasi Zat dengan nilai E° lebih besar mengalami reduksi dan zat yang memiliki nilai E° lebih kecil akan mengalami oksidasi. Reaksi katoda dan anoda: Katoda: (Zn²⁺(aq) + 2e⁻ ⇌ Zn(s)) x 3 | E° = -0,76 volt Anoda: (Al(s) ⇌ Al³⁺(aq) + 3e⁻ ) x 2 | E° = -1,66 volt Maka reaksi dalam sel adalah: Katoda: 3Zn²⁺(aq) + 6e⁻ ⇌ 3Zn(s) | E° = -0,76 volt Anoda: 2Al(s) ⇌ 2Al³⁺(aq) + 6e⁻ | E° = -1,66 volt Reaksi sel: 2Al(s) + 3Zn²⁺(aq) ⇌ 2Al³⁺(aq) + 3Zn(s)
· 1.0 (1)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



