MA
Mrs A
05 Januari 2022 12:04
Iklan
MA
Mrs A
05 Januari 2022 12:04
Pertanyaan
Diketahui reaksi: C2H4 + HBr C2H5Br. Jika diketahui energi ikat: C = C : 609 kJ/mol C – H : 417,06 kJ/mol H – Br : 367,05 kJ/mol C – Br : 285,6 kJ/mol C – C : 349,44 kJ/mol Berapakah kalor yang dibebaskan pada adisi 56 gr gas C2H4 oleh HBr, jika diketahui Ar:C = 12, H = 1
7
1
Iklan
MB
M. Bimba
Mahasiswa/Alumni Universitas Sanata Dharma
19 Januari 2022 17:48
Jawaban terverifikasi
Halo Mrs A, jumlah kalor yang dilepaskan pada reaksi tersebut adalah 152,1 kJ. Ayo simak penjelasan berikut, supaya kamu lebih paham 😃 Entalpi reaksi (∆H) dapat ditentukan dengan beberapa cara, salah satunya dengan data energi ikatan rata-rata. Energi ikatan merupakan energi yang digunakan untuk memutuskan ikatan antar atom dalam satu mol senyawa menjadi atom-atom penyusunnya. Reaksi antara C2H4 dengan HBr dapat dilihat pada gambar terlampir. Perubahan entalpi reaksi diatas dapat ditentukan dari selisih energi ikatan rata-rata reaktan dengan produk. Maka, persamaannya dapat ditulis sebagai berikut: ∆H = ∑Energi ikatan reaktan – ∑energi ikatan produk Untuk mencari jumlah kalor yang dilepaskan, langkah yang dilakukan yaitu: 1. Menentukan ∆H reaksi ∆H = ∑Energi ikatan reaktan – ∑energi ikatan produk ∆H = [(4 × C-H) + (C=C) + (H-Br)] – [(5 × C-H) + (C-C) + (C-Br)] ∆H = [(4 × 417,06 kJ/mol) + (609 kJ/mol) + (367,05 kJ/mol)] – [(5 × 417,06 kJ/mol) + (349,44 kJ/mol) + (285,6 kJ/mol)] ∆H = -76,05 kJ/mol 2. Menentukan mol C2H4 n C2H4 = massa : Mr C2H4 n C2H4 = 56 gram : 28 g/mol n C2H4 = 2 mol 3. Menentukan jumlah kalor (q) ∆H = -q : n q = - ∆H : n q = - ( -76,05 kJ/mol) : 2 mol q = 152,1 kJ Semoga penjelasan diatas bermanfaat ya. Selamat belajar 😎
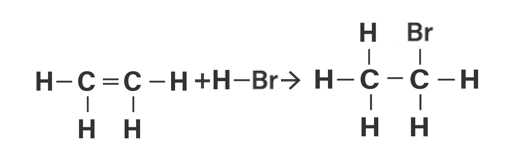
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



