MM
Maria M
15 Januari 2023 05:55
Iklan
MM
Maria M
15 Januari 2023 05:55
Pertanyaan
Dian akan membuat larutan penyangga dengan pH = 9. Larutan penyangga tersebut dibuat dengan cara mencampurkan 100 mL larutan HCl 0,1 M dengan larutan NH4OH 0,2 M. Berapakah volume (dalam mL) larutan NH4OH 0,2 M yang diperlukan untuk membuat larutan penyangga tersebut ? (Diketahui Kb NH4OH = 1 x 10^-5)
1
1
Iklan
SZ
S. Zulaihah
Mahasiswa/Alumni Universitas Negeri Surabaya
07 Februari 2023 12:37
Jawaban terverifikasi
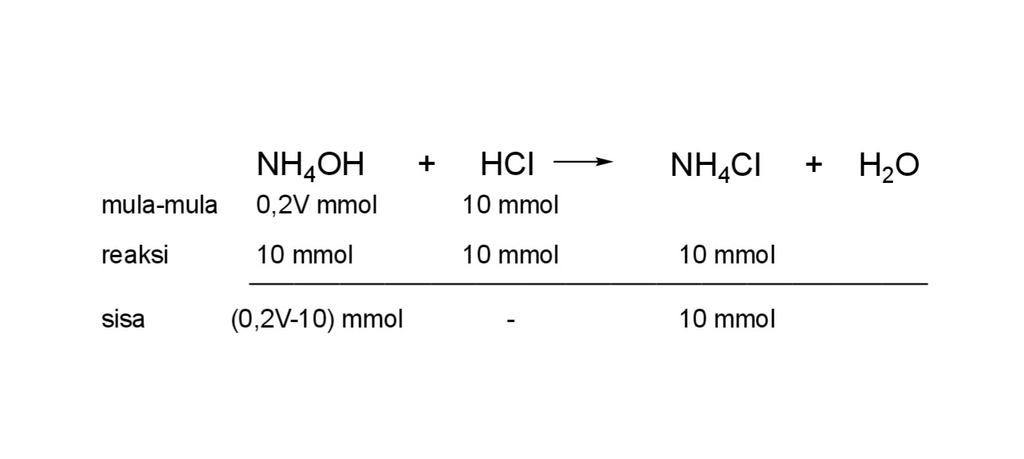
Jawaban yang benar adalah 100 ml. Larutan penyangga merupakan larutan yang dapat mempertahankan nilai pH meskipun ditambah dengan asam kuat, basa kuat maupun dilakukan pengenceran. Terdapat 2 jenis larutan penyangga, yaitu larutan penyangga asam dan larutan penyangga basa. Larutan penyangga basa terdiri dari basa lemah dan asam konjugasinya (garam dari basa lemah tersebut). Contohnya adalah larutan basa lemah NH4OH dengan garam NH4Cl. pH larutan penyangga basa dapat ditentukan dengan rumus sebagai berikut. [OH⁻] = Kb × (mol basa / mol garam) ▪︎menentukan mol HCl mol = M × V mol = 0,1 M × 100 ml mol = 10 mmol ▪︎menentukan mol NH4OH mol = M × v mol = 0,2 M × V mol = 0,2V mmol reaksi yang terjadi adalah sebagai berikut. pH = 9 pOH = 14 - 9 pOH = 5 [OH⁻] = 10⁻⁵ M [OH⁻] = Kb × (mol basa / mol garam) 10⁻⁵ M = 10⁻⁵ × ((0,2V - 10) mmol / 10 mmol) 10 mmol = 0,2V - 10 mmol V = 100 ml Jadi, volume NH4OH yang diperlukan adalah 100 ml.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



