Icha N
06 Desember 2022 08:26
Iklan
Icha N
06 Desember 2022 08:26
Pertanyaan
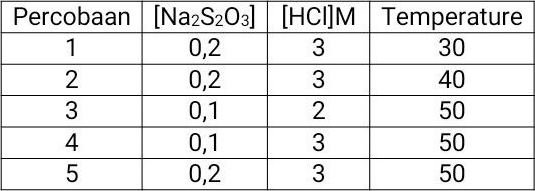
Data percobaan reaksi antara larutan Na2S2O3 dan larutan HCl pada berbagai temperatur dan konsentrasi berbeda : Reaksi paling cepat terdapat pada percobaan nomor ... A. 1 B. 2 C. 3 D. 4 E. 5
14
1
Iklan
S. Susanti
Mahasiswa/Alumni Universitas Jayabaya
12 Desember 2022 09:21
<p>Jawaban : E.</p><p><br> Faktor-faktor yang mempengaruhi laju reaksi yaitu:</p><p>- Konsentrasi</p><p>Semakin tinggi konsentrasi, maka semakin banyak molekul dalam tiap satuan sehingga tumbukan antar molekul intensitasnya makin sering terjadi dan reaksinya berlangsung semakin cepat.</p><p>- Luas permukaan</p><p>Semakin besar luas permukaan partikelnya, maka frekuensi tumbukan semakin tinggi sehingga reaksinya berlangsung semakin cepat. Padatan yang bentuknya serbuk halus memiliki luas permukaan bidang sentuh yang lebih besar dibandingkan dengan padatan yang berbentuk lempeng atau butiran.</p><p>- Suhu</p><p>Semakin tinggi suhu yang digunakan akan menyebabkan energi kinetik (energi gerak partikel) molekul pereaksi semakin besar sehingga kemungkinkan terjadinya tumbukan efektif semakin besar dan reaksi akan berjalan lebih cepat.</p><p>- Katalis</p><p>Adanya katalis dapat mempercepat reaksi dengan cara membentuk tahap - tahap reaksi yang memiliki energi aktivasi lebih rendah.</p><p> </p><p>Pada soal di atas, reaksi paling cepat terdapat pada percobaan nomor 5. Hal ini dikarenakan konsentrasi larutan Na2S2O3 dan larutan HCl yang digunakan paling besar dan suhunya paling tinggi.</p><p><br>Jadi, reaksi paling cepat terdapat pada percobaan nomor 5.</p>
Jawaban : E.
Faktor-faktor yang mempengaruhi laju reaksi yaitu:
- Konsentrasi
Semakin tinggi konsentrasi, maka semakin banyak molekul dalam tiap satuan sehingga tumbukan antar molekul intensitasnya makin sering terjadi dan reaksinya berlangsung semakin cepat.
- Luas permukaan
Semakin besar luas permukaan partikelnya, maka frekuensi tumbukan semakin tinggi sehingga reaksinya berlangsung semakin cepat. Padatan yang bentuknya serbuk halus memiliki luas permukaan bidang sentuh yang lebih besar dibandingkan dengan padatan yang berbentuk lempeng atau butiran.
- Suhu
Semakin tinggi suhu yang digunakan akan menyebabkan energi kinetik (energi gerak partikel) molekul pereaksi semakin besar sehingga kemungkinkan terjadinya tumbukan efektif semakin besar dan reaksi akan berjalan lebih cepat.
- Katalis
Adanya katalis dapat mempercepat reaksi dengan cara membentuk tahap - tahap reaksi yang memiliki energi aktivasi lebih rendah.
Pada soal di atas, reaksi paling cepat terdapat pada percobaan nomor 5. Hal ini dikarenakan konsentrasi larutan Na2S2O3 dan larutan HCl yang digunakan paling besar dan suhunya paling tinggi.
Jadi, reaksi paling cepat terdapat pada percobaan nomor 5.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



